
| A、稀硫酸溶液 | B、蔗糖 |
| C、铜导线 | D、熔融的NaCl |


科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、-(b-a) kJ?mol-1 |
| B、+(b-a) kJ?mol-1 |
| C、(b-a) kJ?mol-1 |
| D、(b+a) kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.0mol/L |
| B、1.5 mol/L |
| C、0.18 mol/L |
| D、0.24mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
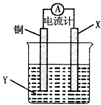 根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,设计如图所示原电池,下列说法错误的是( )
根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,设计如图所示原电池,下列说法错误的是( )| A、X可以是银或石墨 |
| B、电子从铜电极经外电路流向X电极 |
| C、Y是硫酸铜溶液 |
| D、X极上的电极反应式为 O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
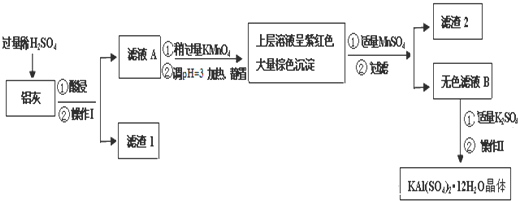
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com