
| A | B |
 制备并收集氨气 |  验证铁的吸氧腐蚀 |
| C | D |
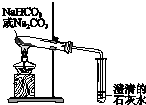 鉴别碳酸钠与碳酸氢钠 | 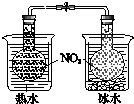 证明温度对平衡移动的影响 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
A、 除去CO的CO2 |
B、 萃取时振荡混合液 |
C、 稀释浓硫酸 |
D、 向试管中滴加液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HA水溶液中微粒浓度大小顺序:c(HA)>c(H+)>c(A-)>c(OH-) |
| B、HA与NH3作用生成的化合物是共价化合物 |
| C、NaA水溶液中:c(Na+)=c(A-)+c(HA) |
| D、稀释0.1mol/LHA水溶液,其电离程度增大,pH也增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)>c(H+) |
| C、0.1mol?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、0.1mol?L-1的硫化钠溶液中:c(OH-)=c(H+)>c(HS-)>c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
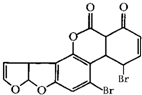 某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )
某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )| A、6mol、4mol |
| B、7mol、4mol |
| C、7mol、5mol |
| D、6mol、5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,0.1mol?L-1 CH3COOH溶液的pH=1 |
| B、铅蓄电池在放电过程中,负极质量增加,正极pH减少 |
| C、反应CO2(g)+C(s)═2CO(g)在低温下不能自发进行,则其△H>0 |
| D、常温下,向AgCl浊液中加入少量NaCl饱和溶液,则c(Ag+)、Ksp(AgCl)均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
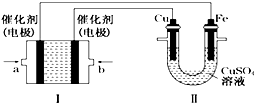 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
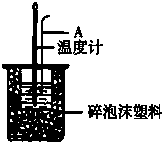 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.| 实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com