
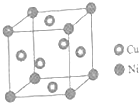
 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:分析 (1)Ni元素原子核外电子数为28,结合能量最低原理书写核外电子排布式;
(2)①SO42-中S原子的孤电子对数=$\frac{6+2-2×4}{2}$=0,价层电子对数=4+0=4;
②Ni2+提供空轨道,NH3中N原子含有孤电子对,二者之间形成配位键;
③PH3分子之间为范德华力,氨气分子之间形成氢键,增大了物质的沸点;NH3分子为三角锥形结构,分子中正负电荷重心不重合,N原子有1对孤对电子,形成3个N-H键,杂化轨道数目为4;
(3)单质铜及镍都属于金属晶体;Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定;
(4)根据均摊法计算晶胞中Ni、Cu原子数目.
解答 解:(1)Ni元素原子核外电子数为28,核外电子排布式为:1s22s22p63s23p63d84s2,3d能级上的未成对电子数为2,
故答案为:1s22s22p63s23p63d84s2;2;
(2)①SO42-中S原子的孤电子对数=$\frac{6+2-2×4}{2}$=0,价层电子对数=4+0=4,离子空间构型为正四面体,
故答案为:正四面体;
②Ni2+提供空轨道,NH3中N原子含有孤电子对,二者之间形成配位键,
故答案为:配位键;N;
③PH3分子之间为范德华力,氨气分子之间形成氢键,分子间作用力更强,增大了物质的沸点,故氨气的沸点高于PH3分子的;
NH3分子为三角锥形结构,分子中正负电荷重心不重合,属于极性分子,N原子有1对孤对电子,形成3个N-H键,杂化轨道数目为4,氮原子采取sp3杂化,
故答案为:高于;氨气分子之间形成氢键,分子间作用力更强;极性;sp3;
(3)单质铜及镍都属于金属晶体,都是由金属键形成的晶体;Cu+的外围电子排布为3d10,呈半充满状态,比较稳定,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定,失去第二个电子更难,元素铜的第二电离能高于镍的,
故答案为:金属;Cu+电子排布呈半充满状态,比较稳定,失电子需要能量高,第二电离能数值大;
(4)晶胞中Ni处于顶点,Cu处于面心,则晶胞中Ni原子数目为8×$\frac{1}{8}$=1、Cu原子数目=6×$\frac{1}{2}$=3,故Cu与Ni原子数目之比为3:1,
故答案为:3:1.
点评 本题考查物质结构和性质,涉及核外电子排布、空间构型与杂化方式判断、配位键、氢键、电离能、晶胞计算等,注意对基础知识的理解掌握,题目难度中等.


科目:高中化学 来源: 题型:选择题
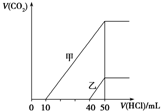
| A. | 原NaOH溶液的物质的量浓度为0.5 mol•L-1 | |
| B. | 当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+═H2O | |
| C. | 乙溶液中含有的溶质是NaOH、NaHCO3 | |
| D. | 乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体 | B. | NH4Cl固体 | C. | NaNO3固体 | D. | CH3COONa固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
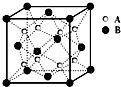 某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )
某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )| A. | B2A | B. | BA2 | C. | B7A4 | D. | B4A7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
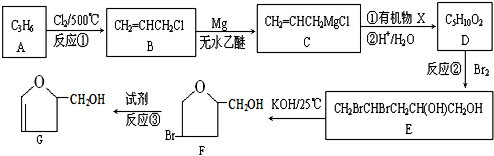

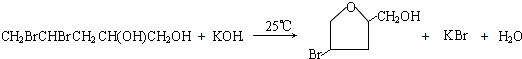 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
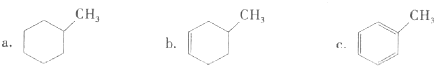
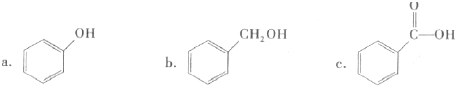
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
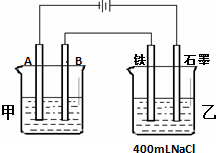 如图所示为相互串联的甲、乙两个电解池,试回答:
如图所示为相互串联的甲、乙两个电解池,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
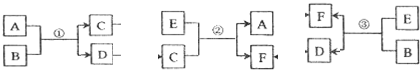
 ;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、水泥、陶瓷属于传统的无机非金属材料 | |
| B. | 聚氯乙烯属于有机材料 | |
| C. | 光导纤维属于新型无机非金属材料 | |
| D. | 玻璃钢属于金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com