
 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成:
 .
. +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.分析 A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知A与氧气反应可以生成乙酸,则A为CH3CHO,由B和C的结构简式可以看出,乙酸分子中的羟基被氯原子取代,发生了取代反应,D与甲醇在浓硫酸条件下发生酯化反应生成E,则E的结构简式为 ,由F的结构简式可知,C和E 在催化剂条件下脱去一个HCl分子得到F,据此解答.
,由F的结构简式可知,C和E 在催化剂条件下脱去一个HCl分子得到F,据此解答.
解答 解:A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知A与氧气反应可以生成乙酸,则A为CH3CHO,由B和C的结构简式可以看出,乙酸分子中的羟基被氯原子取代,发生了取代反应,D与甲醇在浓硫酸条件下发生酯化反应生成E,则E的结构简式为 ,由F的结构简式可知,C和E 在催化剂条件下脱去一个HCl分子得到F,
,由F的结构简式可知,C和E 在催化剂条件下脱去一个HCl分子得到F,
(1)由以上分析可知,A为CH3CHO,与银氨溶液反应的离子方程式为:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O,
故答案为:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O;
(2)由B和C的结构简式可以看出,乙酸分子中的羟基被氯原子取代,发生了取代反应,故答案为:取代反应;
(3)由上面的分析可知,E的结构简式为 ,故答案为:
,故答案为: ;
;
(4)F和过量NaOH溶液共热时反应的化学方程式为: +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O,
+CH3COONa+CH3OH+H2O,
故答案为: +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O;
+CH3COONa+CH3OH+H2O;
(5)G分子的结构中存在苯环、酯基、羟基、碳碳双键,所以能够与溴单质发生加成反应或者取代反应,能够与金属钠反应产生氢气,a和b正确;1molG含有1mol碳碳双键和1mol苯环,所以需要4mol氢气,c错误,G的分子式为C9H6O3,d正确,
故答案为:abd;
(6)E( )的同分异构体很多,除E外符合下列条件:①含苯环且能与氯化铁溶液显色,含有酚羟基,②苯环上有两个取代基,③含酯基,酯基为-CH2OOCH或-OOCCH3或-COOCH3,与酚羟基均有邻、间、对三种位置,故除E外同分异构体有3×3-1=8种,
)的同分异构体很多,除E外符合下列条件:①含苯环且能与氯化铁溶液显色,含有酚羟基,②苯环上有两个取代基,③含酯基,酯基为-CH2OOCH或-OOCCH3或-COOCH3,与酚羟基均有邻、间、对三种位置,故除E外同分异构体有3×3-1=8种,
故答案为:8.
点评 本题考查有机物的推断、有机物结构与性质、有机反应类型、同分异构体等,难度不大,注意掌握有机物官能团的性质和转化,结合反应条件及有机物结构简式进行解答.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
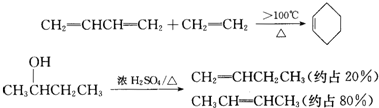

 ;C
;C ;D
;D .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45 | B. | 25 | C. | 29 | D. | 39 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,BN中B元素的化合价为+3;
,BN中B元素的化合价为+3; ,其二氯代物有4种.
,其二氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
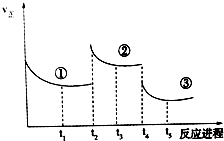 已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )
已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )| A. | t2~t3时间段,平衡向逆反应方向移动 | |
| B. | t4时刻改变的条件是减小压强 | |
| C. | 平衡状态①和②,SO2转化率相同 | |
| D. | 平衡状态①和②,平衡常数K值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A. | 元素③与⑧的金属性相比:前者强于后者 | |
| B. | 上述8种元素中,元素⑤的最高价氧化物对应的水化物酸性最强 | |
| C. | 元素⑦的气态氢化物与元素④的气态氢化物相比较:前者稳定性强,后者沸点高 | |
| D. | 元素①分别与元素②和⑥形成的化合物所含化学键类型不一定完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蓝矾 玻璃 无色的刚玉 | B. | 汽油 液氯 醋酸 | ||
| C. | 石蜡 纯盐酸 王水 | D. | 干冰 铝热剂 铁触媒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、CH4都属于极性键的非极性分子 | |
| B. | C、N、O、F 电负性依次减小 | |
| C. | 基态铜(Cu)原子的电子排布式为[Ar]3d94s2 | |
| D. | 价电子构型为3s23p4的粒子其电子排布图为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④⑤ | C. | ⑤⑥ | D. | ①②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com