
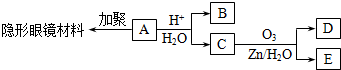
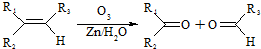
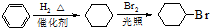
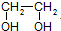
| Cu |
| ”÷ |
| Cu |
| ”÷ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| Ķé »ł | ·ś»ÆĪļ | ĀČ»ÆĪļ | äå»ÆĪļ | µā»ÆĪļ |
| ·Šµć”ę | ·Šµć”ę | ·Šµć”ę | ·Šµć”ę | |
| CH3- | -78.4 | -24.2 | 3.6 | 42.4 |
| CH3-CH2- | -37.7 | 12.3 | 38.40 | 72.3 |
| CH3-CH2-CH2- | 2.5 | 46.60 | 71.0 | 102.4 |
| £ØCH3£©2-CH- | -9.4 | 35.7 | 59.48 | 89.14 |
| CH3-CH2-CH2-CH2- | 32.5 | 78.44 | 101.6 | 130.5 |
| £ØCH3£©2-CH CH2- | 16.0 | 68.7 | 91.7 | 120.4 |
| £ØCH3£©3C- | 12.1 | 52 | 73.25 | 120.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014Ń§ÄźÉ½Ī÷Ź”øßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
·Ö×ÓŹ½ĪŖC6 H13 ClµÄÓŠ»śĪļ·Ö×ÓÖŠ£¬Ėłŗ¬µÄ¼×»łŹż²»æÉÄÜĪŖ£Ø £©
A£®2 B£®3 C£®4 D£®5
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗĶ¬²½Ģā ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com