
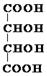
 £®
£®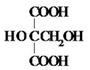 £®MµÄŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠÓŠ4×éĪüŹÕ·å£®
£®MµÄŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠÓŠ4×éĪüŹÕ·å£® ·ÖĪö ¢Ł·Ö×ÓÖŠC”¢HÖŹĮæ·ÖŹż·Ö±šĪŖw£ØC£©=32%£¬w£ØH£©=4%£¬¾Ż“ĖĒó³öOµÄÖŹĮæ·ÖŹż£»
¢Ś1mol¾ĘŹÆĖįÓė×ćĮæµÄNaHCO3·“Ó¦·Å³ö44.8L CO2£¬ĖµĆ÷·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH£¬Óė×ćĮæµÄNa·“Ó¦·Å³ö±źæöĻĀ44.8L H2£¬ĪļÖŹµÄĮæĪŖ2mol£¬ĖµĆ÷·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬øĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓĮæĪŖ150£¬øł¾Żw£ØC£©=32%Ēó³öŗ¬CøöŹż£¬w£ØH£©=4%£¬Ēó³öŗ¬HøöŹż£¬øł¾ŻOµÄÖŹĮæ·ÖŹżĒó³öŃõµÄøöŹż£¬¾Ż“ĖĒó³ö·Ö×ÓŹ½£»
¢ŪøĆ·Ö×ÓÖŠ“ęŌŚČżÖÖ»Æѧ»·¾³²»Ķ¬µÄĢ¼Ō×Ó£¬·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬ÓŠĮ½ÖÖĒāŌ×Ó£¬ĖłŅŌøĆ·Ö×Ó½į¹¹¶Ō³Ę£¬ÓŠČżÖÖ²»Ķ¬µÄHŌ×Ó£®
ÓŠ»śĪļM·Ö×ÓŹ½ĪŖC4H6O6£¬Óė¾ĘŹÆĖįŗ¬ÓŠµÄ¹ŁÄÜĶÅÖÖĄąŗĶŹżÄ棬ŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬ĪŖ¹ŁÄÜĶÅĪ»ÖĆŅģ¹¹£®
½ā“š ½ā£ŗ£Ø1£©¢Ł·Ö×ÓÖŠC”¢HÖŹĮæ·ÖŹż·Ö±šĪŖw£ØC£©=32%£¬w£ØH£©=4%£¬ŌņOµÄÖŹĮæ·ÖŹżĪŖ£ŗ1-32%-4%=64%£»
¢Ś1mol¾ĘŹÆĖįÓė×ćĮæµÄNaHCO3·“Ó¦·Å³ö44.8L CO2£¬ĖµĆ÷·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH£¬Óė×ćĮæµÄNa·“Ó¦·Å³ö±źæöĻĀ44.8L H2£¬ĪļÖŹµÄĮæĪŖ2mol£¬ĖµĆ÷·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬øĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓĮæĪŖ150£¬Ōņŗ¬CøöŹżĪŖ£ŗ$\frac{150”Į32%}{12}$=4£¬ŗ¬HøöŹżĪŖ£ŗ$\frac{150”Į4%}{1}$=6£¬øĆÓŠ»śĪļ·Ö×ÓÖŠŗ¬ÓŠ$\frac{150”Į64%}{16}$=6øöOŌ×Ó£»Ōņ·Ö×ÓŹ½ĪŖC4H6O6£¬
¹Ź“š°øĪŖ£ŗC4H6O6£»2£»2£»
£Ø2£©·Ö×ÓŹ½ĪŖC4H6O6£¬øĆ·Ö×ÓÖŠ“ęŌŚČżÖÖ»Æѧ»·¾³²»Ķ¬µÄĢ¼Ō×Ó£¬·Ö×ÓÖŠŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬ÓŠĮ½ÖÖĒāŌ×Ó£¬ĖłŅŌøĆ·Ö×Ó½į¹¹¶Ō³Ę£¬ÓŠČżÖÖ²»Ķ¬µÄHŌ×Ó£¬¾ĘŹÆĖįµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ÓŠ»śĪļM·Ö×ÓŹ½ĪŖC4H6O6£¬Óė¾ĘŹÆĖįŗ¬ÓŠµÄ¹ŁÄÜĶÅÖÖĄąŗĶŹżÄ棬ŗ¬ÓŠ2øö-COOH”¢2øö-OH£¬ĪŖ¹ŁÄÜĶÅĪ»ÖĆŅģ¹¹£¬ŅņĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬½ÓĮ½øöōĒ»łŹ±²»ĪČ¶Ø£¬»į×Ŗ»ÆĪŖĘäĖūĪļÖŹ£¬ĖłŅŌÖ÷Į“ĪŖ3øöĢ¼£¬Āś×ćøĆĢõ¼žĻĀµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹ĪŖ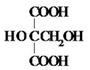 £¬2øö-COOHÉĻµÄĒāŅ»Ńł£¬øĆ·Ö×ÓŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠŗ¬ÓŠ4×éĪüŹÕ·å£®
£¬2øö-COOHÉĻµÄĒāŅ»Ńł£¬øĆ·Ö×ÓŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠŗ¬ÓŠ4×éĪüŹÕ·å£®
¹Ź“š°øĪŖ£ŗ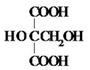 £»4£®
£»4£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņāøł¾ŻĢāÄæŅŖĒó¼ĘĖćĻą¶Ō·Ö×ÓÖŹĮ棬øł¾Ż½į¹¹ĢŲµćŹéŠ“½į¹¹¼ņŹ½£¬°ŃĪÕĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“·½·Ø£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ł¢Ś¢Ü¢Ž | C£® | ¢Ł¢Ś¢Ż¢Ž | D£® | ¢Ū¢Ü¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe3+”¢Cl-”¢NO3- | B£® | K+”¢HCO3-”¢OH- | C£® | Na+”¢HCO3-”¢H+ | D£® | NH4+”¢H+”¢SO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĢ¼ĖįĒāøĘČÜŅŗÖŠ¼ÓČėÉŁĮæÉÕ¼īČÜŅŗ£ŗCa2++2HCO3-+20H-ØTCaCO3”ż+CO32-+H2O | |
| B£® | µāĖ®ÖŠĶØČė×ćĮæµÄ S02£ŗI2+SO2+2H2OØT2I-+S042-+4H+ | |
| C£® | ĻņĀČ»ÆĀĮČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė®£ŗAl3++4NH3•H2OØTA1O2-+4NH4++2H2O | |
| D£® | ŌŚĒæ¼īČÜŅŗÖŠ“ĪĀČĖįÄĘÓėFe£Ø0H£©3·“Ӧɜ³ÉNa2FeO4£ŗ3ClO+2Fe£ØOH£©3ØT2FeO32-+3Cl-+H2O+4H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×Ó | B£® | Ō×Ó | ||
| C£® | ŃōĄė×ÓÓėŅõĄė×Ó | D£® | ŃōĄė×ÓÓė×ŌÓɵē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3COOC3H7 | B£® | CH3COOC2H5 | C£® | CH3COONa | D£® | CH3CH2Br |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com