
分析 B的次外层电子数为2,能够形成最高正价为+4,则B为C元素;C、D、A原子次外层电子数均为8,则C、D、A处于第三或四周期,核电荷数按B、C、D、A顺序增大,且A的最高化合价为+1,则A处于第四周期,为K元素;C、D只能处于第二周期,C最高正价为+5,则C为P元素;D最高正价为+7,则D为Cl元素,据此进行解答.
解答 解:B的次外层电子数为2,能够形成最高正价为+4,则B为C元素;C、D、A原子次外层电子数均为8,则C、D、A处于第三或四周期,核电荷数按B、C、D、A顺序增大,且A的最高化合价为+1,则A处于第四周期,为K元素;C、D只能处于第二周期,C最高正价为+5,则C为P元素;D最高正价为+7,则D为Cl元素,
根据分析可知,A为K、B为C、C为P、D为Cl,
故答案为:K;C;P;Cl.
点评 本题考查了位置、结构与性质关系的应用,题目难度中等,明确原子结构与元素周期表、元素周期律的关系为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
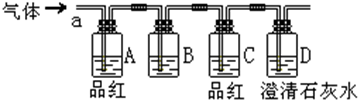
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2 | B. | CH3CH═CHCH3 | C. | CH3CH═CH2 | D. | CH2═CHCH═CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
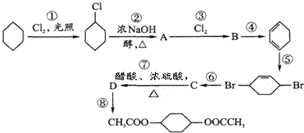 从环己烷可制备1,4-环己二醇二醋酸酯,下列过程是有关的8步反应(其中所有无机产物都已略去):
从环己烷可制备1,4-环己二醇二醋酸酯,下列过程是有关的8步反应(其中所有无机产物都已略去):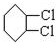 ,C
,C ,D
,D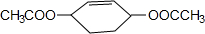 .
.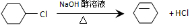 ;
;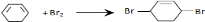 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一电离能越大的原子越容易得到电子 | |
| B. | 同周期元素从左到右第一电离能一定增大 | |
| C. | 同周期元素电负性从左到右越来越大 | |
| D. | 金属元素的电负性一定小于非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 短周期元素Q、R、T、W在元素周期表中的位置如图:其中T所处的周期序数与主族序数相等,请回答下列问题
短周期元素Q、R、T、W在元素周期表中的位置如图:其中T所处的周期序数与主族序数相等,请回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com