
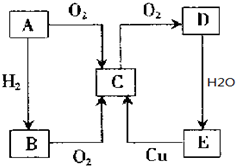
 A、B、C、D、E五种物质有如图所示的转化关系,且物质A是一种淡黄色的固体单质,C气体能够使品红溶液褪色.
A、B、C、D、E五种物质有如图所示的转化关系,且物质A是一种淡黄色的固体单质,C气体能够使品红溶液褪色.分析 A、B、C、D、E五种物质,且物质A是一种淡黄色的固体单质,C气体能够使品红溶液褪色,结合转化关系可知,A为S,C为 SO2,B为H2S,D为SO3,E为H2SO4.
解答 解:A、B、C、D、E五种物质,且物质A是一种淡黄色的固体单质,C气体能够使品红溶液褪色,结合转化关系可知,A为S,C为 SO2,B为H2S,D为SO3,E为H2SO4.
(1)A为S,C为SO2,E为H2SO4,
故答案为:S;SO2;H2SO4;
(2)①刚刚制成的湿粉丝,常常挂在房中用SO2来熏制,这是利用了SO2的漂白作用,
②实验室中可用酸性高锰酸钾来检验SO2的存在,利用的是SO2的还原性,
故答案为:漂白;还原;
(3)①将 H2SO4 溶液敞口放置在空气中,浓硫酸具有吸水性,其质量会增大,质量分数会减小,
故答案为:增大;减小;
②H2SO4 溶液表现吸水性时,可作干燥剂,浓硫酸浓郁氨气反应,浓硫酸还原强氧化性,能氧化硫化氢,浓硫酸不与二氧化硫反应,
故答案为:C;
③用蘸有浓 H2SO4 溶液的玻璃棒在木板上写字,字迹一会儿就变黑,说明浓 H2SO4溶液具有脱水性,
故答案为:脱水;
④浓 H2SO4 溶液具有强氧化性,在加热的条件下能与铜单质反应的化学方程式:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
⑤稀的E溶液常常用来洗涤金属铁表面铁锈(Fe2O3),这是利用了E的酸性,有关的化学方程式:3H2SO4+Fe2O3═Fe2(SO4)3+3H2O,
故答案为:酸;3H2SO4+Fe2O3═Fe2(SO4)3+3H2O.
点评 本题考查无机物推断,涉及硫元素单质化合物性质,题目比较基础,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
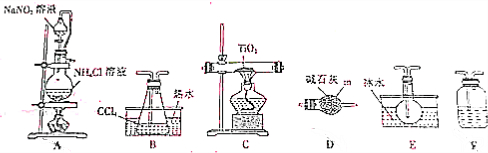
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与 TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,加热时能被氧气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤①需要使用普通漏斗 | B. | 步骤②要使用分液漏斗 | ||
| C. | 步骤③要用到坩埚 | D. | 步骤④需要蒸馏装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(A2)=0.4 mol•L-1•s-1 | B. | υ(B2)=0.8 mol•L-1•s-1 | ||
| C. | υ(C)=0.6 mol•L-1•s-1 | D. | υ(D)=0.6 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
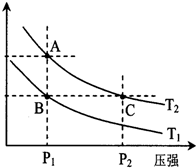 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com