
| A. | SO2是硫及某些含硫化合物在空气中燃烧的产物 | |
| B. | SO2具有漂白性,可以使品红溶液褪色 | |
| C. | SO2溶于水后生成H2SO4 | |
| D. | SO2是一种大气污染物 |
分析 A.S单质及含硫化合物可与氧气反应;
B.二氧化硫具有漂白性,其漂白性具有不稳定的特点;
C.二氧化硫为亚硫酸的酸酐,二氧化硫与水反应生成亚硫酸;
D.二氧化硫有毒.
解答 解:A.S单质及含硫化合物可与氧气反应,则SO2是硫及某些含硫化合物在空气中燃烧的产物,故A正确;
B.二氧化硫与品红化合生成无色物质,则SO2具有漂白性,可以使品红溶液褪色,故B正确;
C.二氧化硫与水反应生成亚硫酸,故C错误;
D.SO2是一种大气污染物,二氧化硫可导致酸雨的发生,它主要来自于化石燃料的燃烧,故D正确;
故选C.
点评 本题考查了元素化合物知识,熟悉二氧化硫的性质是解题关键,注意二氧化硫漂白原理及其污染性,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:计算题
 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| B. | 乙醇和汽油都是可再生资源,应大力推广使用“乙醇汽油” | |
| C. | 加入明矾使海水中的盐分沉淀可以使海水淡化,解决“淡水供应危机” | |
| D. | 要尽快发现地球上的有用物质,加大开采速度,加快社会发展 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

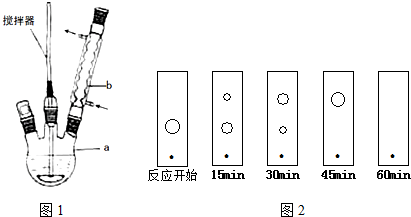
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 氯化铝溶液中加入过量的氨水 Al3++4NH3•H2O=AlO2-+4NH4++2H2 O | |
| C. | 钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ | |
| D. | 纯碱溶液中通入二氧化碳:CO32-+CO2+H2O=2HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 用铜片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面出现一层铜 | |
| C. | 电解精炼铜,粗铜中所含Ni、Fe,Zn等杂质,电解后以单质形式沉积槽底 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com