
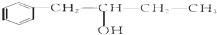
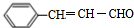
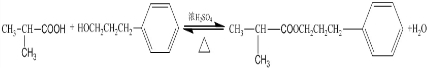
 ,该反应类型为酯化反应:
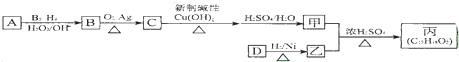
,该反应类型为酯化反应:分析 结合已知信息③得,A反应生成醇B,B被氧气氧化生成醛C,醛被新制氢氧化铜氧化,再酸化得到甲,则甲为羧酸,甲与乙生成丙,由丙的分子式可知,丙属于酯,乙属于醇,甲的相对分子质量为88,去掉1个-COOH后剩余烃基式量为88-45=43,则烃基为-C3H7,故甲为C3H7COOH,又它的核磁共振氢谱显示有3组峰,所以甲为(CH3)2CHCOOH,则C的结构简式为(CH3)2CHCHO,B的结构简式为(CH3)2CHCH2OH,A的结构简式为(CH3)2C=CH2,结合丙、甲分子式可知乙分子式为C9H12O,又乙为香醇的同系物,由于丙中只有两个甲基,又甲分子中含有2个甲基,故乙中无甲基,1mol D可以和2mol H2反应生成乙,D又可以发生银镜反应,则含有醛基,则D为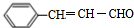 ,乙为
,乙为 ,据此解答;
,据此解答;
解答 解:结合已知信息③得,A反应生成醇B,B被氧气氧化生成醛C,醛被新制氢氧化铜氧化,再酸化得到甲,则甲为羧酸,甲与乙生成丙,由丙的分子式可知,丙属于酯,乙属于醇,甲的相对分子质量为88,去掉1个-COOH后剩余烃基式量为88-45=43,则烃基为-C3H7,故甲为C3H7COOH,又它的核磁共振氢谱显示有3组峰,所以甲为(CH3)2CHCOOH,则C的结构简式为(CH3)2CHCHO,B的结构简式为(CH3)2CHCH2OH,A的结构简式为(CH3)2C=CH2,结合丙、甲分子式可知乙分子式为C9H12O,又乙为香醇的同系物,由于丙中只有两个甲基,又甲分子中含有2个甲基,故乙中无甲基,1mol D可以和2mol H2反应生成乙,D又可以发生银镜反应,则含有醛基,则D为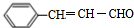 ,乙为
,乙为 ,
,
(1)根据以上分析得,A为(CH3)2C=CH2,名称是:2-甲基丙烯,故答案为:2-甲基丙烯;
(2)根据以上分析得,B的结构简式为(CH3)2CHCH2OH,其分子式为C4H10O,故答案为:C4H10O;
(3)根据以上分析得,C为(CH3)2CHCHO,与新制Cu(OH)2悬浊液反应的化学方程式为:(CH3)2CHCHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$(CH3)2CHCOONa+Cu2O↓+3H2O,
故答案为:(CH3)2CHCHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$(CH3)2CHCOONa+Cu2O↓+3H2O;
(4)根据以上分析得,D为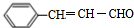 ,故答案为:
,故答案为: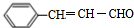 ;
;
(5)根据以上分析,甲为(CH3)2CHCOOH,乙为 ,甲与乙反应的化学方程式为:
,甲与乙反应的化学方程式为: ,反应类型为酯化反应,
,反应类型为酯化反应,
故答案为: ;酯化反应;
;酯化反应;
(6)甲为(CH3)2CHCOOH的同分异构体中含有“ ”结构,含有羧基或酯基,符合条件的同分异构体结构有:CH3CH2CH2COOH、HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOCH2CH3、CH3CH2COOCH3,共有5种,核磁共振氢谱为3组峰.且峰面积之比为6:1:1的为HCOOCH(CH3)2;故答案为:5;HCOOCH(CH3)2.
”结构,含有羧基或酯基,符合条件的同分异构体结构有:CH3CH2CH2COOH、HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOCH2CH3、CH3CH2COOCH3,共有5种,核磁共振氢谱为3组峰.且峰面积之比为6:1:1的为HCOOCH(CH3)2;故答案为:5;HCOOCH(CH3)2.
点评 本题考查有机物推断,需要学生对给予的信息进行利用,是常见题型,注意根据转化关系判断物质含有的官能团,结合E的相对分子质量确定E的结构简式,再结合有机物分子式与转化关系进行推断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ①③⑤⑧ | C. | ②④⑥⑦ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个H+的质量为1g | |
| B. | 32g O2中含有2NA个O原子 | |
| C. | 2 L 0.5mol/LNa2SO4溶液中含NA个Na+ | |
| D. | 标准状况下,1 molH2O中含有10NA个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0X10-10 | 5.4X10-13 | 8.3X10-17 | 2.0X10-41 | 2.0X10-12 |
| A. | 20℃时.AgCl饱和溶液和Ag2CrO4饱和溶液中.Ag+物质的量浓度由大到小的顺序是Ag2CrO4>AgCl | |
| B. | 20℃时,向相同浓度的KCl和KBr混合溶液中逐滴滴加AgNO3溶液.会先生成浅黄色沉淀 | |
| C. | 20℃时,向相同浓度的KCl和KBr混合溶液中逐滴滴加AgNO3溶液,当两种沉淀共存时.c(Br-):C(C1-)=2.7×10-3 | |
| D. | 在100ml AgCl、AgBr、AgI饱和的混合溶液中加入足量浓AgNO3溶液,产生沉淀AgI质量最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
| B. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| C. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| D. | 标准状况下,22.4 L氧气作氧化剂时转移电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氩的原子序数 | B. | 氩原子的质量数 | ||
| C. | 氩元素的相对原子质量 | D. | 氩原子的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 左、下方区域的金属元素 | |
| B. | 右、上方区域的非金属元素 | |
| C. | 金属元素与非金属元素分界线附近的元素 | |
| D. | 过渡元素中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com