
碳、硅两元素广泛存在于自然界中.请回答下列问题:
(1)基态14C原子的核外存在________对自旋方向相反的电子,硅原子的电子排布式为__________。
(2)晶体硅的结构与全刚石非常相似。晶体硅硅中硅原子的杂化方式为_______杂化;金刚石、晶体硅和金刚砂(碳化硅)的熔点由高到低的顺序为_____________。
(3)科学研究结果表明,碳的氧化物CO2能够与H2O借助子太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中δ键和π键的个数比是_______。
(4)碳单质有多种形式,其中C60、石墨烯与金刚石晶体结构如图所示:
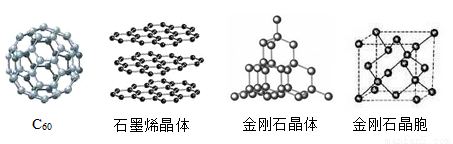
①C60、石墨烯与金刚石互为_________。
②C60形成的晶体是分子晶体,C60分子中含有12个五边形和20个六边形,碳与碳之间既有单键又有双键,已知C60分子所含的双键数为30,则C60分子中_______个C—C 键(多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2)。在石墨烯晶体中,每个C原子连接______个六元环;在金刚石晶体中,每个C原子连接的最小环也为六元环,六元环屮最多有_______个C原子在同一平面。
③金刚石晶胞含有______个碳原子。若碳原子的半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=______a,列式表示碳原子在晶胞中的空间占有率为_______(不要求计算结果)。
科目:高中化学 来源:2016-2017学年天津市高一3月学生学业能力调研(文)化学试卷(解析版) 题型:选择题
根据元素的单质和化合物的性质,判断元素非金属性强弱的依据可以是
A. 元素最高价氧化物对应的水化物的碱性的强弱
B. 元素最高价氧化物对应的水化物的酸性的强弱
C. 元素的单质与碱反应置换出氢的难易
D. 元素的单质与氧气生成化合物的难易
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二学业水平测试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A. 铁粉与稀H2SO4反应:2Fe+6H+=2Fe3++3H2↑
B. Na2CO3溶液与足量盐酸反应:CO32-+2H+=CO2↑+H2O
C. Cu(OH)2固体与稀H2SO4反应: OH-+H+= H2O
D. 铝片与NaOH溶液反应:Al+OH-+H2O=AlO2-+ H2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一下学期第一次月考理科综合化学试卷(解析版) 题型:推断题
I:A、B、C三种气体都是大气的主要污染物,A是一种单质,其水溶液具有杀菌消毒作用,B是形成酸雨的主要污染物,C是硝酸工业和汽车尾气中的有害物质之一,能与水反应。请回答下列问题:
(1)A用于工业上制取漂白粉的化学方程式:________________.
(2)B在一定条件下与氧气反应的化学方程式:________________。
(3)A、B都能分别使品红溶液褪色,但两者水溶液混合后却不能使品红溶液褪色且溶液酸性增强:________________(用离子方程式表示),其中氧化剂和还原剂分别是________、________(填化学式),
(4)C与水反应的化学方程式:_________________。
II:汽车尾气(含CO、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排放管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体,并促进二氧化硫的转化.
(1)汽车尾气中导致酸雨形成的主要物质是_______________.
(2)写出在催化剂的作用下CO跟NO反应的化学方程式: ___________________.
(3)实验室一般用________(填化学式)溶液吸收除去尾气二氧化氮。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3﹣═3Fe3++NO↑+3H2O
B. 铜与稀硝酸反应:3Cu+8 H++2NO3﹣═3Cu2++2NO↑+4H2O
C. 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl﹣ Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+2Fe(OH)3═2FeO42﹣+3Cl﹣+H2O+4H+
查看答案和解析>>
科目:高中化学 来源:2017届河南省豫南九校高三下学期质量考评七理综化学试卷(解析版) 题型:选择题
如图所示.在一定电压下用惰性电极电解由等物质的量浓度的FeC12、HCl组成的混合溶液。己知在此电压下,阴、阳离子根据放电能力顺序,都可能在阳极放电,下列分析正确的是

A. C1电极上的电极反应式为:2H2O+2e-=2OH-+H2↑
B. C1电极处溶液首先变黄色
C. C2电极上可依次发生的电极反应为:Fe2+-e-=Fe3+,2Cl--2e-=Cl2↑
D. 当C1电极上有2g物质生成时,就会有2NA个电子通过溶液发生转移
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三二模理科综合化学试卷(解析版) 题型:填空题
(1)下列有关说法正确的是_________________。
A.用金属的电子气理论能合理地解释金属易腐蚀的原因
B.手性催化剂只催化或者主要催化一种手性分子的合成
C.草酸二甲酯分子中σ键和π键个数比为6:1
D.MgCO3的热稳定性强于BaCO3
E.根据火山喷出的岩浆中冷却时ZnS比HgS先析出,能判断ZnS的晶格能大于HgS
(2)已知SbCl3、SbCl5、SnCl4的熔点依次为73.5℃、2.8℃、-33℃。依据上述实验事实回答:
①SnCl4中Sn的杂化类型为________,SbCl5的晶体类型为_______,SbCl3的空间构型为____________。
②实验测得在极性溶剂中SbCl5的溶解度比SbCl3的溶解度小得多,其主要原因是___________。
(3)人们一直致力于人工固氮的研究,以获得廉价的氮肥。科学家先后提出并合成了固氮酶的多种模拟物。其中一类是含Mo(钼)、Fe、S原子的类立方体结构,如下图所示:

图中所有实线均代表化学键,左右两边对称,各含一个类立方体的结构。每个类立方体含有4个Fe原子、4个S原子,它们位于立方体的8分顶点,且同种原子不相邻。(已知元素电负性分别为:S—2.5 Fe—1.8 Mo—1.8)
①Mo与Cr是同族元素,并且位于相邻周期,写出基态Mo原子的价电子的轨道表达式为_____________。
②钼是一种人体必需的微量元素。工业上可用辉钼矿(MoS2)焙烧除硫得三氧化钼,写出该过程的化学方程式___________________。
③上述一个类立方体中4个Fe原子所在的顶点连接所构成的空间几何体为_____________。
④在类立方体结构中,一种最近的S原子和S原子间距离为apm,该结构的密度为_______g/cm3(已知NA,只需列式,无需化简)。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三适应性月考(六)理综化学试卷(解析版) 题型:选择题
“电芬顿法”除去水体里有机污染物的原理如图所示,发生电芬顿反应:Fe2++H2O2== Fe3++OH-+·OH,生成的羟基自由基(·OH)能降解有机污染物。下列说法正确的是
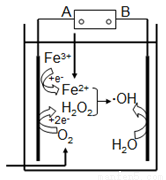
A. 电源的A极是正极,B极是负极
B. 阴极上O2、Fe3+、H2O2得电子发生还原反应
C. 阳极上发生电极反应:H2O-e-==•OH+H+
D. 常温常压下,消耗22.4LO2,可以产生4mol·OH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.阿伏加德罗常数的准确值应为6.02×1023mol-1
B.标准状况下,17g氨气的体积为22.4L/mol
C.常温常压条件下,3.6gH2O所含氢原子数为0.4NA
D.浓度为0.1 mol/LNa2CO3溶液中,Na+数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com