
| A. | 氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O | |
| B. | 在标准状况下,17.92L SO2气体通入到1L 1mol/L的NaOH溶液中:4SO2+5OH-═SO32-+3HSO3-+H2O | |
| C. | 向碳酸氢镁溶液中加入过量的澄清石灰水:Mg2++2HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O | |
| D. | 用KI-淀粉试纸和食醋检验食用盐是否为加碘食盐:IO3-+5I-+6H+═3I2+3H2O |
分析 A.离子方程式两边负电荷不相等,违反了电荷守恒;
B.计算出二氧化硫、氢氧化钠的物质的量,然后判断反应生成物即可;
C.澄清石灰水过量,反应生成氢氧化镁沉淀;
D.醋酸为弱酸,离子方程式中醋酸不能拆开.
解答 解:A.氯气通入冷的氢氧化钠溶液中,反应生成次氯酸钠、氯化钠和水,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故A错误;
B.氢氧化钠的物质的量=1L×1mol/L=1mol,标况下17.92L SO2的物质的量=$\frac{17.92L}{22.4L/mol}$=0.8mol,氢氧化钠部分过量,反应生成Na2SO3和NaHSO3的混合物,令二者物质的量分别为xmol、ymol,根据Na元素和C元素守恒,则:$\left\{\begin{array}{l}{x+y=0.8}\\{2x+y=1}\end{array}\right.$,解得:x=0.2、y=0.6,n(SO32-):n(HSO3-)=02mol:0.6mol=1:3,反应的离子方程式为:4SO2+5OH-═SO32-+3HSO3-+H2O,故B正确;
C.在碳酸氢镁溶液中加入过量氢氧化钙溶液,氢氧化镁更难溶,反应生成氢氧化镁沉淀,正确的反应为:2Ca2++Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CaCO3↓+2H2O,故C错误;
D.用KI-淀粉试纸和食醋检验食用盐是否为加碘食盐,醋酸需要保留分子式,正确的离子方程式为:IO3-+5I-+6CH3COOH═3I2+3H2O+6CH3COO-,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液:NH4+、Fe3+、CO32-、SO42- | |
| B. | 含有大量AlO2-的溶液中:Fe2+、Cu2+、Cl-、Na+ | |
| C. | 中性溶液中:Fe3+、Al3+、Na+、K+、NO3- | |
| D. | Na2S溶液中:K+、NH4+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 铝热剂、福尔马林、水玻璃、漂白粉均为混合物 | |
| C. | 一定条件下,1mol苯甲醛最多能与3molH2反应 | |
| D. | 乙醇、乙酸均能与NaOH稀溶液反应,因为分子中均含有官能团“-OH” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含Fe2+ | B. | 只含Cu2+、Fe2+ | ||
| C. | 只含Fe3+、Fe2+ | D. | 只含Fe3+、Cu2+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
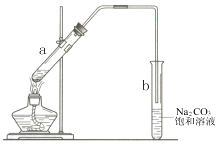
| A. | 向试管a中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 | |
| B. | 试管b中导气管下端管口不能浸入液面的目的是防止实验过程中产生倒吸现象 | |
| C. | 实验时加热试管a的目的之一是及时将乙酸乙酯蒸出 | |
| D. | 试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 | |
| B. | 用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol•L-1)通常需要用容量瓶等仪器 | |
| C. | 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解 | |
| D. | 用pH=1的盐酸配制100 mL pH=2的盐酸所需全部玻璃仪器有100 mL容量瓶、烧杯、玻璃棒、胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| B. | 一定条件下用含1mol FeCl3的溶液制备Fe(OH)3胶体,产生NA个Fe(OH)3胶粒 | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ②③⑤ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com