


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| 1 |
| 2 |
| 1 |
| 2 |
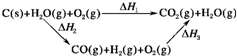
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013吉林省吉林一中高二下学期期中考试化学试卷(带解析) 题型:填空题
党的十七大报告指出:“加强能源资源节约和生态环境保护,增强可持续发展能力,坚持节约资源和保护环境的基本国策,发展环保产业.”
(1)下列有关做法不符合上述要求的是________.
| A.将煤液化、气化,提高燃料的燃烧效率 |
B.安装汽车尾气催化转化装置,使之反应:4CO+2NO2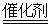 4CO2+N2 4CO2+N2 |
| C.大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃烧电池汽车 |
| D.在水力发电、火力发电、核能发电和风力发电中要大力发展火力发电 |
 CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为: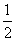 O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②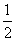 O2(g)===CO2(g) ΔH=-283.0 kJ/mol ③
O2(g)===CO2(g) ΔH=-283.0 kJ/mol ③查看答案和解析>>
科目:高中化学 来源:2012-2013吉林省高二下学期期中考试化学试卷(解析版) 题型:填空题
党的十七大报告指出:“加强能源资源节约和生态环境保护,增强可持续发展能力,坚持节约资源和保护环境的基本国策,发展环保产业.”
(1)下列有关做法不符合上述要求的是________.
A.将煤液化、气化,提高燃料的燃烧效率
B.安装汽车尾气催化转化装置,使之反应:4CO+2NO2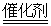 4CO2+N2
4CO2+N2
C.大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃烧电池汽车
D.在水力发电、火力发电、核能发电和风力发电中要大力发展火力发电
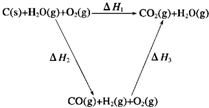
(2)将煤转化为水煤气的主要化学反应为
C(s)+H2O(g) CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol ①
H2(g)+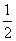 O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
CO(g)+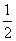 O2(g)===CO2(g)
ΔH=-283.0 kJ/mol
③
O2(g)===CO2(g)
ΔH=-283.0 kJ/mol
③
请回答:
①根据以上数据,写出C(s)与H2O(g)反应的热化学方程式:_____________________________________.
②水煤气不仅是优良的气体燃料,也是重要的有机化工原料,CO和H2在一定条件下可以合成:a.甲醇;b.甲醛;c.甲酸;d.乙酸.试分析当CO和H2按1∶1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com