
 在硬质玻璃管中的A,B,C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示).向左端导入Cl2,在B处加热,可观察到A处棉球呈
在硬质玻璃管中的A,B,C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示).向左端导入Cl2,在B处加热,可观察到A处棉球呈

科目:高中化学 来源: 题型:
| 操作① |
| 加试剂A |
| 饱和Na2CO3溶液 |
| ① |
| 盐酸 |
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
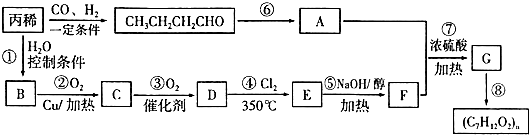
| 350℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 3名同学在用氯酸钾和二氧化锰混合加热制取氧气的过程中,发现生成的气体有刺激性气味,针对这一“异常现象”进行了实验探究及分析.
3名同学在用氯酸钾和二氧化锰混合加热制取氧气的过程中,发现生成的气体有刺激性气味,针对这一“异常现象”进行了实验探究及分析.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁不需要特殊处理就有很强的抗腐蚀能力 |
| B、手机中锂离子电池属于二次电池 |
| C、“地沟油”经过加工处理制得肥皂或生物柴油,可以实现厨余废物的合理利用 |
| D、以NaClO为有效成分的漂白液可以作为游泳池的消毒剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com