
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B.在此饱和溶液中加水,KSP(AgCl)增大 |
| C.在此饱和溶液中加浓的Na2S溶液,生成黑色沉淀 |
| D.向AgCl饱和溶液中加入NaCl固体,c(Ag+)不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 .盐碱地(含较多NaCl、Na2CO3)不利于作物生成,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
.盐碱地(含较多NaCl、Na2CO3)不利于作物生成,通过施加适量石膏(CaSO4)可以降低土壤的碱性。 加入石膏降低土壤碱性的反应原理 ;
加入石膏降低土壤碱性的反应原理 ; 请分析水垢中的CaSO4转化为CaCO3的原理 ;
请分析水垢中的CaSO4转化为CaCO3的原理 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgCl=AgI=Ag2S | B.AgCl<AgI<Ag2S |
| C.AgCl>AgI>Ag2 S | D.AgI>AgCl>Ag2S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.MnS的Ksp比CuS的Ksp大 | ||
| B.该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| C.往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大 | ||
D.该反应的平衡常数K=
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
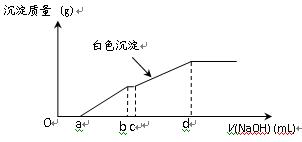
A.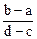 | B.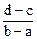 |
C.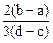 | D.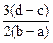 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com