
【题目】十九大报告中指出“持续实施大气污染防治行动,打赢蓝天保卫战”。SO2为大气污染物,研究它的性质对治理具有重要意义。在铝基氧化铜作催化剂时,可利用天然气脱除二氧化硫,并回收单质硫(熔点为112.8℃,沸点为444.6℃)。
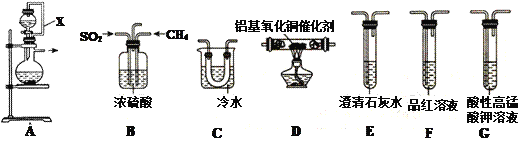
(1)①装置中导管X的作用是:______________________________。
②用装置A制取SO2,则试剂的组合最好是_________(填字母)。
a. 18.4 mol/L H2SO4+Cu b. 4 mol/L HNO3+Na2SO3 c. 60% H2SO4+K2SO3
③水与Al4C3在装置A中制取甲烷,其化学方程式为:________________。
(2)利用制得的CH4和SO2并结合B~G装置验证反应:CH4+2SO2 .![]() 2S+CO2+2H2O生成的单质S和CO2。
2S+CO2+2H2O生成的单质S和CO2。
①B装置有三个作用,分别是________________________、充分混合CH4和SO2、观察气泡以便调节CH4和SO2的流速比约为1∶2。
②实验装置依次连接的合理顺序为B、_____________________(每个装置只用一次)。
③证明有CO2产生的现象为_____________________________。
④G装置中发生反应的离子方程式为_____________________________。
【答案】使液体顺利滴入烧瓶中 c Al4C3+12H2O==4Al(OH)3↓+3CH4↑ 干燥CH4、SO2 D、C、G、F、E F中品红不褪色,澄清石灰水变浑浊 2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+
【解析】
(1)①由于装置A的蒸馏烧瓶中产生气体,使其中的压强增大,在分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是平衡压强,使液体顺利滴入烧瓶中。②a项,装置A为固液不加热装置,“18.4mol/LH2SO4+Cu”制取SO2需要加热,故不适合;b项,“4 mol/LHNO3+Na2SO3”发生氧化还原反应,+4价S被氧化成+6价,得不到SO2,故不适合;c项,“60%H2SO4+K2SO3”制取SO2适合强酸制弱酸原理,故合适。③水与Al4C3制取甲烷,根据原子守恒还生成Al(OH)3,故化学方程式为:Al4C3+12H2O=4Al(OH)3↓+3CH4↑。
(2)①如图CH4和SO2的反应需要高温条件下在硬质玻璃管中进行,所以B中浓硫酸除了充分混合CH4和SO2、观察气泡以便调节CH4和SO2的流速比约为1∶2之外,还有干燥CH4和SO2的作用。②根据实验目的是验证CH4和SO2反应生成的单质S和CO2,装置C冷却得到固体S单质,用E装置中澄清石灰水验证CO2,为防止SO2对验证实验的干扰,必须先依次通过酸性高锰酸钾和品红溶液,将其除尽,综上分析实验装置依次连接的合理顺序为B、D、C、G、F、E。③若F中品红不褪色,则说明SO2已经被除尽,E中澄清石灰水变浑浊则能证明该实验有CO2产生。④G装置中,酸性高锰酸钾与SO2发生氧化还原反应,+7价Mn被还原为+2价,+4价S被氧化为+6价,离子方程式为:2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+。


科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.用水分离四氯化碳和酒精的混合物
B.蒸馏完毕时,先再停止加热,关闭冷凝水
C.配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸 馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释
D.将放在称量纸上称取的NaOH固体在烧杯中溶解,待冷却后,再转移至容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应中,属于可逆反应的一组是( )
A. 2H2O![]() 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2![]() 2H2O
2H2O
B. NH3+CO2+H2O=NH4HCO3,NH4HCO3![]() NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑
C. H2+I2![]() 2HI,2HI
2HI,2HI![]() H2↑+I2↑
H2↑+I2↑
D. 2Ag+Br2![]() 2AgBr,2AgBr
2AgBr,2AgBr![]() 2Ag+Br2
2Ag+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出CH4和Cl2在光照的条件下生成CH3Cl的化学反应方程式_________
(2)写出如图所示原电池的电极方程式:
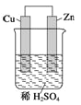
负极:_______________________
正极:_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)下列说法中正确的是__(填序号).
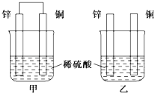
A.甲、乙均为化学能转变为电能的装置
B.甲中铜为正极,乙中铜为负极
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中的pH值均增大
(2)在相同时间内,两烧杯中产生气泡的速率:甲__乙(填“>”、“<”或“=”).
(3)写出甲池中负极反应的电极反应式为:_______________________________。
(4)当甲中产生3.36L(标准状况)气体时,理论上通过导线的电子数目为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题是2007年“两会”的重要议题,保护环境是公民的责任和义务。下列说法正确的是
A.大量使用含磷洗涤剂会带来白色污染
B.减少使用氟氯代烷的目的是为了减少酸雨
C.大量开采地下水,矿产资源,以满足社会经济发展的需求
D.氢燃料和电池汽车的使用,可以有效减少城市空气污染。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com