
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ③④ |
分析 ①植物只能够吸收以化合态存在的氮元素;
②氮气氧气在放电时生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸,硝酸与矿物盐生成硝酸盐;
③大豆、蚕豆、豌豆等豆科植物可利用与其共生的根瘤菌固氮,杨梅可利用和其共生的菌根固氮,水生蕨类植物红萍,能利用叶腔中与其共生的固氮鱼腥藻固氮,固氮蓝藻能固氮.
④氮被固定后经植物吸收储存在植物体内,动物以植物为食而获得氮并转化为动物蛋白质.
解答 解:①空气中的氮气,不能被生物直接吸收,故①错误;
②氮气氧气在放电时生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸,硝酸与矿物盐生成硝酸盐,故②正确;
③不是所有植物都有生物固氮作用,能够固定氮的植物,不全都是通过根部吸收,③错误;
④氮被固定后经植物吸收储存在植物体内,动物以植物为食而获得氮并转化为动物蛋白质,故④正确;
故选:②④.
点评 本题考查了氮的固体,熟悉基本概念即可解答,侧重考查学生对基本知识的掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸亚铁铵晶体要用冷水洗涤,而阿斯匹林过滤后则须用无水酒精洗涤 | |
| B. | 食醋总酸含量的测定实验中,若滴定终点没有控制好,即NaOH溶液滴加过量,则必须重做实验 | |
| C. | 火柴头中的氯元素检验的实验中,将火柴头(未燃烧)浸于水中,片刻后取少量溶液,加AgNO3溶液、稀硝酸,若出现白色沉淀,证明有氯元素 | |
| D. | 毒物误入口内,可将5~10mL稀硫酸铜溶液加入一杯温水中内服,人工促使呕吐出毒物后送医院 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
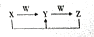 A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图.
A、B、C、D、E均是常见短周期元素,其在周期表中的位置如图. | A | |||||
| B | C | D | |||
| E | |||||
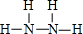
 ,其中Y和Z在水溶液中存在的微粒种类相同.
,其中Y和Z在水溶液中存在的微粒种类相同.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
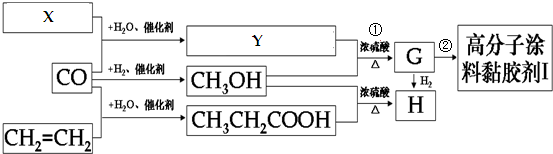
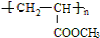
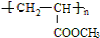 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
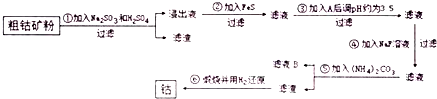
 铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物.
铜合金是人类使用最早的金属材料.铜在化合物中的常见化合价有+l、+2 等,故能形成多种铜的化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com