
分析 在2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO的化学反应中,Mg元素化合价由0价升高为+2价,O元素化合价由0价降低为-2价,以此解答该题.
解答 解:在2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO的化学反应中,氧元素由0价降低为-2价,氧原子得到电子的总数为4,则镁原子失去电子的总数为4,1mol Mg参与反应时转移电子的物质的量为2mol.
故答案为:-2;4;4;2mol.
点评 本题考查氧化还原反应,为高频考点,侧重学生的分析能力的考查,注意把握氧化还原反应的特征和反应的实质以及相关概念,把握元素化合价的变化,难度不大.


科目:高中化学 来源: 题型:选择题
 下列有关实验的操作、现象和原理,正确的是( )
下列有关实验的操作、现象和原理,正确的是( )| A. | ②④⑤ | B. | ③⑤⑥ | C. | ③⑤⑥⑦ | D. | ②⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L的NaCl溶液是指此溶液中含有1 mol NaCl | |
| B. | 从1L 0.5mo1/L的NaCl溶液中取出100 mL溶液,其物质的量浓度变为0.1mol/L | |
| C. | 0℃时,1molC12的体积约为22.4L | |
| D. | 1mol/L的CaCl2溶液中,Cl-的物质的量浓度为2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
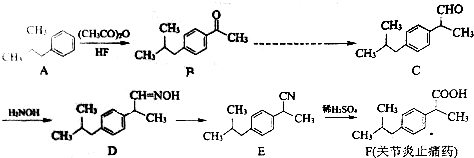
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯中溶液转移到容量瓶中时,未洗涤烧杯 | |
| B. | 移液时,有少量液体溅出 | |
| C. | 定容时,俯视刻度线 | |
| D. | 定容摇匀后发现液面下降,继续加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铁制容器可盛装冷的浓硫酸,因为常温下铁和浓硫酸不反应 | |
| B. | Na2O2用作呼吸面具的供氧剂 | |
| C. | 欲鉴别FeCl2溶液、AlCl3溶液和AgNO3溶液,向3种待测液中分别滴加足量氨水 | |
| D. | 铝热反应需提供一定的能量引发,因为铝热反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
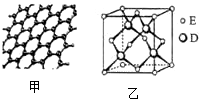 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com