
| A. | NaHSO3溶液中存在:c(Na+)>c(HSO3-)>c(OH-)>c(H+)>c(SO32-) | |
| B. | 当吸收液呈中性时:c(Na+)=2c(SO32-)+c(HSO3-) | |
| C. | 含等物质的量的Na2SO3和NaHSO3的溶液中,阴离子数目相等 | |
| D. | Na2SO3和NaHSO3都能抑制水的电离 |
分析 A.NaHSO3溶液pH<7,该溶液中亚硫酸根离子电离大于水解;
B.当吸收液呈中性时,c(H+)=c(OH-),依据溶液中电荷守恒分析;
C.含等物质的量的Na2SO3和NaHSO3的溶液中,亚硫酸根离子水解程度大于亚硫酸氢根离子,亚硫酸钠溶液显碱性,亚硫酸氢钠溶液显酸性;
D.Na2SO3和溶液显碱性是亚硫酸根离子水解促进水的电离,NaHSO3都溶液显酸性,亚硫酸氢根离子电离大于水解,能抑制水的电离;
解答 解:A.NaHSO3溶液pH<7,该溶液中亚硫酸根离子电离大于水解,溶液中离子浓度大小c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)>c(H2SO3),故A错误;
B.当吸收液呈中性时,c(H+)=c(OH-),溶液中存在的电荷守恒为c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-)得到c(Na+)=2c(SO32-)+c(HSO3-),故B正确;
C.含等物质的量的Na2SO3和NaHSO3的溶液中,亚硫酸根离子水解程度大于亚硫酸氢根离子,亚硫酸钠溶液显碱性,亚硫酸氢钠溶液显酸性,溶液中氢氧根离子数目不同,溶液中阴离子数目不相等,故C错误;
D.Na2SO3和溶液显碱性是亚硫酸根离子水解促进水的电离,NaHSO3都溶液显酸性,亚硫酸氢根离子电离大于水解,电离出的氢离子能抑制水的电离,故D错误;
故选B.
点评 本题考查了电解质溶液中离子浓度大小比较,电荷守恒和物料守恒的计算应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 决定化学反应速率的主要因素是参加反应的物质的性质 | |
| B. | 升高温度可使吸热反应的反应速率增大.使放热反应的反应速率减小 | |
| C. | 等量的甲烷在纯氧气中燃烧的火焰的温度比在空气中燃烧时高 | |
| D. | 用物质的量浓度相同的盐酸分别与相同质量的石灰石块和石灰石粉末反应,石灰石快反应速率慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
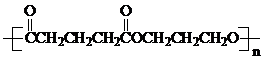 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
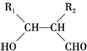
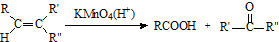
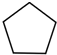 .
. .
.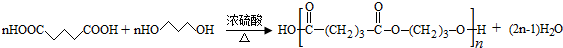 .
. .
.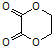 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 立即撤离火灾现场并拨打119报警 | |
| B. | 若逃生通道被堵,应迅速转移到窗口边或阳台上等待救援 | |
| C. | 若被困在室内,应立即封堵火、烟的进口,并站在室内最高处等待救援 | |
| D. | 若被困在火灾现场,应尽可能贴近地面向火势小、烟雾少的方向撤离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 通过化学变化可以实现16O与18O间的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质一定是离子化合物,弱电解质一定是共价化合物 | |
| B. | 强电解质一定是易溶化合物,弱电解质一定是难溶化合物 | |
| C. | SO3溶于水后水溶液导电性很强,所以SO3是强电解质 | |
| D. | 强电解质与弱电解质的本质区别是在水溶液中能否完全电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
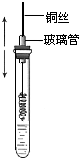 某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:
某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
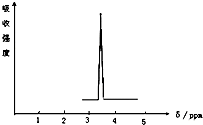 (1)某有机物含碳85.7%、氢14.3%,向80g含溴5%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重81.4g.
(1)某有机物含碳85.7%、氢14.3%,向80g含溴5%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重81.4g.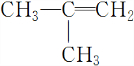 .任选其中一种写出其生成高聚物的化学方程式
.任选其中一种写出其生成高聚物的化学方程式 (或
(或
 +3HNO3
+3HNO3
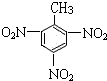 +3H2O.
+3H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com