
【题目】在a LAl2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;如加入足量强碱并加热可得到c molNH3,则原溶液中的Al3+浓度(mol/L)为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】C
【解析】
根据反应SO42-+Ba2+=BaSO4↓计算溶液中的SO42-离子的物质的量,根据离子方程式NH4++OH-![]() NH3↑+H2O计算NH4+的物质的量,再根据c=
NH3↑+H2O计算NH4+的物质的量,再根据c=![]() 计算出溶液中硫酸根离子、铵根离子的浓度,最后利用电荷守恒来计算原溶液中的Al3+浓度。
计算出溶液中硫酸根离子、铵根离子的浓度,最后利用电荷守恒来计算原溶液中的Al3+浓度。
由混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀,则根据SO42-+Ba2+=BaSO4↓可知n(SO42-)=b mol;由加入足量强碱并加热可得到c mol NH3,根据NH4++OH-![]() NH3↑+H2O可知n(NH3)=c mol,由于溶液不显电性,设原溶液中的Al3+的物质的量为x,由电荷守恒可知,3x+c=2b,所以x=
NH3↑+H2O可知n(NH3)=c mol,由于溶液不显电性,设原溶液中的Al3+的物质的量为x,由电荷守恒可知,3x+c=2b,所以x=![]() mol,由于溶液的体积是a L,所以原溶液中Al3+的物质的量浓度c(Al3+)=
mol,由于溶液的体积是a L,所以原溶液中Al3+的物质的量浓度c(Al3+)=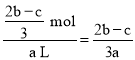 mol/L,故合理选项是C。
mol/L,故合理选项是C。


科目:高中化学 来源: 题型:
【题目】我省近年来以铁矿石为原料的产业发展迅猛,下列有关说法正确的是
A.以焦炭和铁矿石为原料炼铁的原理是用焦炭直接还原化合态的铁
B.据报道,庐江磁性材料产生“磁”力无穷,磁性氧化铁的化学式是![]()
C.为证明某铁矿石中存在铁离子,可将铁矿石溶于硝酸后,再加KSCN溶液
D.利用铁矿石制得的能除去污水中的![]() ,可知相同条件下,
,可知相同条件下,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是
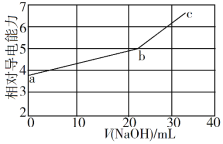
A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发酵法制酒精的过程可粗略表示如下:
①(C6H10O5)n+nH2O![]() nC6H12O6 ②C6H12O6
nC6H12O6 ②C6H12O6![]() 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
(1)上述化学方程式中(C6H10O5)n可能表示_____ ____(填物质名称);
(2)C6H12O6名称是_________,常用_____ ____试剂来检验其存在;
(3)为检验苹果成熟过程中发生了反应①,可在青苹果汁中滴加碘酒,溶液呈_________色,向熟苹果汁中加入Cu(OH)2悬浊液,加热,反应生成____ ____(填实验现象);
(4)下列作用不属于水解反应的是_________
A.吃馒头时多咀嚼后有甜味
B.淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色
C.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
D.油脂与氢氧化钠溶液共煮后可以制得肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.按系统命名法,有机物![]() 可命名为3,7-二甲基-4-乙基辛烷
可命名为3,7-二甲基-4-乙基辛烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段为![]() 的高聚物,其单体是甲醛和苯酚
的高聚物,其单体是甲醛和苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是
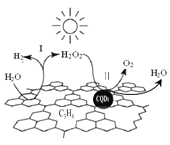
A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
含量/mgL-1 | 9360 | 83 | 160 | 1100 | 16000 | 1200 | 118 |
(1)海水显弱碱性的原因是(用离子方程式表示):____________,该海水中Ca2+的物质的量浓度为__________mol/L 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过,电极均为惰性电极。
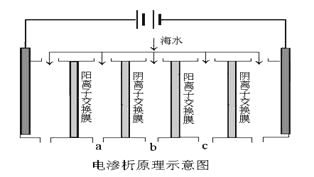
① 开始时阳极的电极反应式为________________。
② 电解一段时间,____极(填“阴”或“阳”)会产生水垢,其成份为_____(填化学式)。
③ 淡水的出口为a、b、c中的__________出口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图所示:
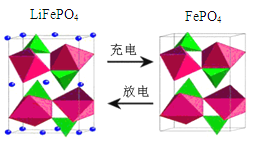
该电池电解质为能传导 Li+的固体材料。
上面左图中的小黑点表示_____(填粒子符号),充电时该电极反应式为_______。
(4)利用海洋资源可获得MnO2 。MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾。该制备过程中消耗相同条件下氯气和空气的体积比为_________(空气中氧气的体积分数按20%计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1)为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
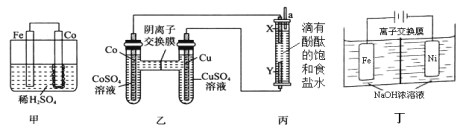
①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号)。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B.S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
C.Al(s)![]() AlCl3(aq)
AlCl3(aq)![]() Al(OH)3(s)
Al(OH)3(s)
D.N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com