
下列各组液体混合物,用分液漏斗能分开的是( )
A.溴乙烷和氯仿 B.乙醇和水
C.甲苯和水 D.苯和溴苯
科目:高中化学 来源: 题型:
关于反应过程中的先后顺序,下列评价正确的是( )
|
| A. | 向浓度都为0.1mol/L的FeCl3和CuCl2加入铁粉,溶质CuCl2首先与铁粉反应 |
|
| B. | 向过量的Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成 |
|
| C. | 向浓度都为0.1mol/L Na2CO3和NaOH溶液通入CO2气体,NaOH首先反应 |
|
| D. | 向浓度都为0.1mol/L的FeCl3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)鉴别KCl溶液和K2CO3的试剂是________,离子方程式为
________________________________________________________________________。
(2)除去FeCl2溶液中混有的FeCl3用________,离子方程式为
________________________________________________________________________。
(3)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)________________________________________________________________
________________________________________________________________________。
(4)有A、B、C、D四种无色气体,①A能使湿润的红色石蕊试纸变蓝;②一定条件下,A可以与B反应生成C,C遇空气变为红棕色;③D与A混合生成白烟;④D的浓溶液与软锰矿(主要成分是MnO2)在加热条件下反应可制取黄绿色气体E;按要求回答下列问题:
a.写出实验室制A气体的化学反应方程式
________________________________________________________________________。
b.写出②化学反应方程式
_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若1 mol 某气态烃CxHy完全燃烧,需用3 mol O2,则( )
A.x=2,y=2 B.x=2,y=4
C.x=3,y=6 D.x=3,y=8
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A可作为植物生长调节剂,为便于使用,通常将其制成化合物
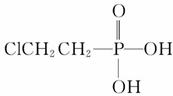 D( ),D在弱酸性条件下会缓慢释放出A。合成D的一种
D( ),D在弱酸性条件下会缓慢释放出A。合成D的一种
方法及各物质间转化关系如图所示:
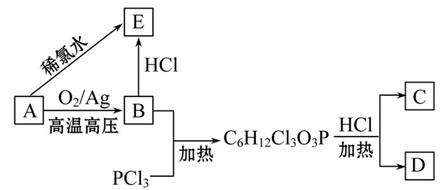
请回答下列问题:
(1)A的名称是_________,A与氯气反应可生成C,C的名称是_________;
(2)经测定E中含有氯元素,且E可以与乙酸发生酯化反应,则E的结构简式为_________,由A直接生成E的反应类型是_________;
(3)在弱酸性条件下,D与水反应生成A的化学方程式为______________________;
(4)写出E的两个同分异构体的结构简式__________________。
A可作为植物生长调节剂,则A为乙烯;
由第(2)问“E中含有氯元素,且E可以与乙酸发生酯化反应”知E中含有氯元素和羟基,结合E可以由乙烯与稀氯水反应得到推知E为ClCH2CH2OH,可以认为是CH2=CH2与HO—Cl加成的产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:3X(g)+Y(g) nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·L-1·min-1,则n的值
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·L-1·min-1,则n的值
为 ( )
A.4 B.3 C.2 D.1
查看答案和解析>>
科目:高中化学 来源: 题型:
电化学在日常生活中有广泛的应用,下列说法或做法正确的是( )
A.暴雨后遭洪水浸泡的铁门生锈是因为发生化学腐蚀
B.白铁皮(铁镀锌)表面有划损时,不能阻止铁被腐蚀
C.废弃的干电池不能随意丢弃,但可以土埋处理
D.不能将铁制自来水管与铜制水龙头连接
查看答案和解析>>
科目:高中化学 来源: 题型:
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的反应热等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列两组物质的熔点高低(填“>”或“<”):
SiC Si,Si SiO2。
(2)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)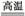 Si(s)+4HCl(g),(已知1 mol Si中含有2 mol Si—Si键)则2 mol H2生成高纯硅需 (填“吸收”或“放出”)能量 kJ。
Si(s)+4HCl(g),(已知1 mol Si中含有2 mol Si—Si键)则2 mol H2生成高纯硅需 (填“吸收”或“放出”)能量 kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com