
【题目】某无色溶液中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:下列结论正确的是
离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:下列结论正确的是
步骤 | 操作 | 现象 |
| 用pH试纸检验 | 溶液的pH大于7 |
| 向溶液中滴加氯水,再加入 |
|
| 向 | 有白色沉淀产生 |
| 过滤,向滤液中加入 | 有白色沉淀产生 |
A.肯定含有离子的![]() 、
、![]() 、
、![]()
B.肯定没有的离子是![]() 、
、![]()
C.可能含有的离子是![]() 、
、![]() 、
、![]()
D.不能确定的离子是![]() 、
、![]() 、
、![]()
【答案】A
【解析】
依据题干中的条件,用pH试纸检验,测得溶液pH大于7,溶液呈碱性,说明一定有弱酸根离子,则含有![]() ,无
,无![]() ;溶液中滴加氯水后萃取,萃取层呈橙色证明原溶液含溴离子; 稀硝酸具有强氧化性,能氧化亚硫酸根离子,向
;溶液中滴加氯水后萃取,萃取层呈橙色证明原溶液含溴离子; 稀硝酸具有强氧化性,能氧化亚硫酸根离子,向![]() 所得的水溶液中加入
所得的水溶液中加入![]() 溶液和稀
溶液和稀![]() ,有白色沉淀生成,说明溶液中可能含硫酸根离子,过滤,向滤液中加入
,有白色沉淀生成,说明溶液中可能含硫酸根离子,过滤,向滤液中加入![]() 溶液和稀
溶液和稀![]() ,有白色沉淀生成,证明是氯离子,但
,有白色沉淀生成,证明是氯离子,但![]() 加入氯水加入了氯离子,不能确定是否含氯离子。
加入氯水加入了氯离子,不能确定是否含氯离子。
A.根据以上分析溶液中一定含有![]() 、
、![]() ,故A正确;
,故A正确;
B.根据以上分析可知:溶液中一定含有![]() ,故B错误;
,故B错误;
C.根据以上分析可知:无色溶液中可能含有![]() 、
、![]() ,一定含有
,一定含有![]() ,故C错误;
,故C错误;
D.依据电荷守恒,溶液中一定含![]() ,故D错误;
,故D错误;
答案:A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是![]()
A.饱和氯水中滴加NaOH至溶液呈中性:![]()
B.100mL![]() 的
的![]() 溶液和200
溶液和200![]() 的
的![]() 溶液所含的
溶液所含的![]() 相同
相同
C.![]() 的一元酸和
的一元酸和![]() 的一元强碱等体积混合后的溶液;
的一元强碱等体积混合后的溶液;![]()
D.常温下,![]() 、浓度均为
、浓度均为![]() 。
。![]() 的
的![]() 、
、![]() COONa混合溶液
COONa混合溶液![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一端呈螺旋状的铜丝放在酒精灯上加热,铜丝表面生成黑色的___,再迅速把铜丝插入成盛有乙醇的试管中,看到铜丝表面___,反复多次,试管中有带___气味的___生成;所涉及反应的化学方程式为___,反应中乙醇被___(填“氧化”或“还原”),铜丝的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuO有氧化性,能被NH3还原,为验证此结论,设计如下实验。
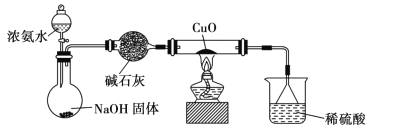
有关该实验的说法正确的是
A.反应时生成一种无污染的气体NO
B.NH3与CuO反应后生成的红色物质可能是Cu
C.装浓氨水的装置名称是分液漏斗,只能用作分液操作
D.烧杯中硫酸的作用是防倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pC类似pH,如图为CO2的水溶液中加入强酸或强碱溶液后,平衡时溶液中各种组分的pC - pH图。依据图中信息,下列说法不正确的是
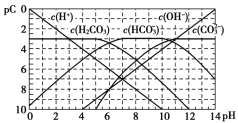
A.![]() 不能在同一溶液中大量共存
不能在同一溶液中大量共存
B.H2CO3电离平衡常数![]()
C.人体血液里主要通过碳酸氢盐缓冲体系(![]() )可以抵消少量酸或碱,维持pH =7.4,但当过量的酸进入血液中时,血液缓冲体系中的
)可以抵消少量酸或碱,维持pH =7.4,但当过量的酸进入血液中时,血液缓冲体系中的![]() 最终将变大
最终将变大
D.pH =9时,溶液中存在关系![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),向20mL0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液 , 根据图示判断,下列说法正确的是( )
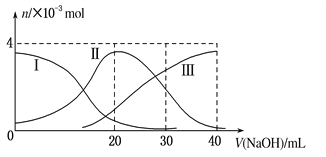
A. H2A在水中的电离方程式是:H2A===H++HA-;HA-![]() H++A2-
H++A2-
B. 当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C. 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
D. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
过渡元素有特殊性能常用于合金冶炼,p区元素用于农药医药、颜料和光电池等工业。
(l)量子力学把电子在原子核外的一种空间运动状态称为一个原子轨道,电子除空间运动状态外,还有一种运动状态叫作_______
(2)基态亚铜离子中电子占据的原子轨道数目为____。
(3)Cr3+可以与CN -形成配离子,其中Cr3+以d2sp3方式杂化,杂化轨道全部用来与CN -形成配位键,则Cr3+的配位数为 ______,1 mol该配离子中含有_______ molσ键。
(4)单晶硅可由二氧化硅制得,二氧化硅晶体结构如图所示,在二氧化硅晶体中,Si、O原子所连接的最小环为____元环,则每个O原子连接________个最小环。
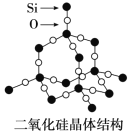
(5)与砷同周期的p区元素中第一电离能大于砷的元素有 ________(填元素符号);请根据物质结构的知识比较酸性强弱亚砷酸(H3AsO3,三元酸)____HNO3(填>,=,<)。
(6) Zn与S形成晶胞结构如图所示,晶体密度为p g/cm3,则晶胞中距离最近的Zn、S之间的核间距离是____pm。(NA表示阿伏加德罗常数,用含p、NA等的代数式表示)
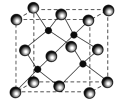
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作或实验现象的解释(方程式)正确的是
A.除去Na2CO3溶液中的Na2SO4,加入适量Ba(OH)2溶液后,过滤:Ba2++![]() =BaSO4↓
=BaSO4↓
B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2=Ag2S↓+2Cl
C.Na2O2在潮湿的空气中放置一段时间,变成白色黏稠物:2Na2O2+2CO2=2Na2CO3+O2
D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀: 2![]() +Ca2++2OH=CaCO3↓+
+Ca2++2OH=CaCO3↓+![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿(主要成分为Al2O3,还含少量Fe2O3、SiO2等)为主要原料生产金属铝的工艺流程如图:下列说法错误的是
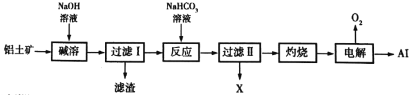
A.碱溶过程发生复杂的氧化还原反应
B.过滤1的滤渣中含Fe2O3、SiO2等
C.X主要溶质是Na2CO3
D.产生Al和O2的电解过程通常使用助熔剂Na3AlF6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com