
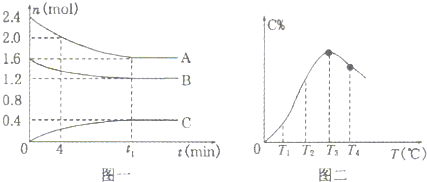
 在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系.一定条件下,A、B、C三种物质物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示.下列分析错误的是( )
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系.一定条件下,A、B、C三种物质物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示.下列分析错误的是( )| A. | 0-4min时,A的平均反应速率为0.01mol/(L•min) | |
| B. | 图二中T3、T4对应曲线上的点都处于化学平衡状态 | |
| C. | 由T1向T2变化时,V正>V逆 | |
| D. | 该反应的正反应为吸热反应 |
分析 根据图1知,随着反应的进行,A和B的物质的量减少,C的物质的量增大,则A和B是反应物,C是生成物,
反应过程中,物质的量的变化量之比等于其计量数之比,所以A、B和C的计量数之比=(2.4-1.6)mol:(1.6-1.2)mol:(0.4-0)mol=0.8mol:0.4mol:0.4mol=2:1:1,当反应达到T3时,再升高温度C的含量降低,则正反应是放热反应,该反应的方程式为:2A(g)+B(g)?C(g)△H<0;
A.根据v=$\frac{△c}{△t}$计算平均反应速率;
B.0到T3是平衡的建立,T3后是平衡的移动;
C.由T1向T2变化时,C的含量增大,则平衡向正反应方向移动;
D.当达到平衡状态后,升高温度平衡向吸热反应方向移动,根据C的含量变化判断反应热.
解答 解:根据图1知,随着反应的进行,A和B的物质的量减少,C的物质的量增大,则A和B是反应物,C是生成物,反应过程中,物质的量的变化量之比等于其计量数之比,所以A、B和C的计量数之比=(2.4-1.6)mol:(1.6-1.2)mol:(0.4-0)mol=0.8mol:0.4mol:0.4mol=2:1:1,当反应达到T3时,再升高温度C的含量降低,则正反应是放热反应,该反应的方程式为:2A(g)+B(g)?C(g)△H<0.
A.0~4分钟时,A的平均反应速率v=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{(2.4-2.0)mol}{10L}}{4min}$=0.01mol/(L•min),故A正确;
B.0到T3是平衡的建立,T3后是平衡的移动,T3后的所有点都是对应温度下的平衡状态,所以图二中T3、T4对应曲线上的点都处于化学平衡状态,故B正确;
C.由T1向T2变化时,C的含量增大,平衡向正反应方向移动,则正反应速率大于逆反应速率,故C正确;
D.该反应正反应是放热反应,故D错误;
故选D.
点评 本题考查了化学平衡图象的分析,正确推断可逆反应及反应热是解本题关键,注意图2中探究反应热时,必须是当反应达到平衡状态后再改变温度来确定反应热,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 用单位体积的溶剂中所含溶质的物质的量来表示溶液组成的物理量叫溶质的物质的量浓度 | |
| B. | 常温常压下,氢气分子和氧气分子本身的大小对于气体体积影响可以忽略不计 | |
| C. | 不同的气体,若体积不同,则它们所含的分子数一定不同 | |
| D. | 气体摩尔体积是指1mol任何气体所占的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用碘单质在酒精中的溶解度大,用酒精把碘水中的碘单质萃取出来 | |
| B. | 要分离汽油和水,最好使用蒸馏法 | |
| C. | 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾,可以利用溶解度随温度变化的差异采取结晶法 | |
| D. | 要从在实验室加热氯酸钾和二氧化锰的混合物中分离得到二氧化锰,应使用分液漏斗进行分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
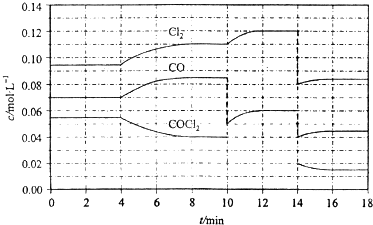
| A. | < | B. | = | ||
| C. | > | D. | 条件不足,无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.2NA | |
| B. | 标准状况下,33.6L SO3中含有硫原子的数目为1.5NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目小于0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com