
| 试剂 | ①H2SO4②KMnO4 ③KI ④AgNO3 ⑤淀粉溶液 |
| 发生的现象 | A:生成白色沉淀 B:溶液显蓝色 C:溶液紫色褪去 |


科目:高中化学 来源: 题型:
| 操作 | 现象 |
| ①取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| ②过滤,测漂粉精溶液的pH | pH试纸先变蓝,最后褪色 |
③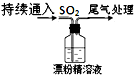 |
液面上方出现白雾;稍后,出现浑浊,溶液变为黄绿色;最终,产生大量白色沉淀,黄绿色褪去. |
| A、Cl2和Ca(OH)2制取漂粉精的化学方程式是:2Cl2+2Ca(OH)2→CaCl2+Ca(ClO)2+2H2O |
| B、pH试纸颜色的变化说明漂粉精溶液具有碱性、漂白性 |
| C、液面上方出现白雾,白雾中一定只含HCl |
| D、最后,产生大量白色沉淀,黄绿色褪去,推测白色沉淀主要是CaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、固体煤经处理变为气体燃料后,提高了燃烧效率,可以减少SO2和烟尘的排放,有利于“节能减排” | B、推广利用微生物发酵技术,用植物秸秆、动物粪便等生产沼气可以代替石油液化气 | C、海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 | D、研制开发燃料电池汽车,降低机动车尾气污染,可有效防治光化学烟雾的发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2012年12月31日,山西一化工厂发生苯胺泄漏事故,苯胺对环境有污染 | B、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可以发生水解反应 | C、从海水中可以得到NaCl,电解熔融NaCl可制备Na | D、医疗上的血液透析利用了胶体的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 | C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
| A、C7H16 |
| B、C7H14O2 |
| C、C8H18 |
| D、C8H18O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钾钠合金和钠的熔点 | B、纯水在80℃和25℃的pH | C、等物质的量的N2和H2在一定条件下反应,两者的转化率 | D、25℃时pH=11的Na2CO3溶液和pH=11的NaOH溶液中的水的电离度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com