
| A. | pH>7的溶液一定是碱溶液 | |
| B. | pH试纸先用水润湿不一定会对测定结果造成偏差 | |
| C. | pH试纸应不经润湿直接放入待测液中 | |
| D. | 将酚酞溶液滴加到pH<7的溶液中会变红 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入水时,平衡向左移动 | |
| B. | 加入少量CH3COONa固体,平衡向右移动 | |
| C. | 加入少量NaOH固体,平衡向右移动 | |
| D. | 加入少量0.01mol•L-1HCl溶液,溶液中c(H+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单辨认有味的化学药品时,将瓶口远离鼻子,用手在瓶口上方扇动,稍闻其味即可 | |
| B. | 处置实验过程产生的剧毒药品废液,稀释后用大量水冲净 | |
| C. | 金属钠着火不能用水灭火,应使用干砂灭火 | |
| D. | 危险化学品包括:爆炸品、易燃物质、自燃自热物质、氧化性气体、加压气体等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g铁与足量的氯气反应失去的电子为0.2 mol | |
| B. | 25℃、pH=0的溶液中,Al3+、NH4+、NO3-、Fe2+可以大量共存 | |
| C. | 2Fe3++Fe═3Fe2+成立说明氧化性:Fe3+>Fe2+ | |
| D. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,将浓硫酸缓慢地沿着量筒内壁倒入蒸馏水中,并用玻璃棒进行搅拌 | |
| B. | 实验室的酒精灯着火时,应该立即往上撒水 | |
| C. | 实验室制氧气,组装好装置后,应该先检查装置的气密性 | |
| D. | 过滤时,若滤液浑浊,则将滤液放入蒸发皿中进行蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
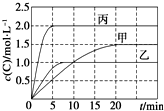 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | 1.0 L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A. | 10min内甲容器中反应的平均速率v(A)=0.025 mol•L-1•min-1 | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | 若平衡时保持温度不变,改变容器体积平衡不移动 | |
| D. | T1℃,起始时甲容器中充入0.5 mol A、1.5 mol B,平衡时A的转化率为25% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com