
| A.焓减小的反应通常是自发的,能够自发进行的反应都是焓减小的反应 |
| B.熵增加的反应通常是自发的,能够自发进行的反应都是熵增加的反应 |
| C.由焓判据和熵判据组合而成的复合判据,更适合于过程自发性的判断 |
| D.焓减小的反应通常是自发的,因此不需要任何条件即可发生 |
科目:高中化学 来源:不详 题型:单选题
| A.NH4NO3溶于水虽然吸热,但其溶于水是自发过程 |
| B.加热液体(温度高于沸点)会自发转变成气体,可用焓变解释 |
| C.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小 |
| D.要正确判断化学反应能否自发进行,要综合考虑反应的ΔH和ΔS。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g);△H<0,下列研究目的和示意图相符的是
2NH3(g);△H<0,下列研究目的和示意图相符的是| | A | B | C | D |
| 研究目的 | 压强对反应的 影响(P2>P1) | 温度对反应的影响 | 增加N2的浓度对反应的影响 | 催化剂对反应的 影响 |
| 图示 |  | 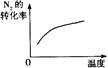 | 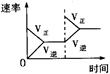 | 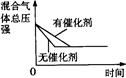 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
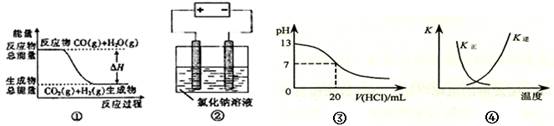
A.图①表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)中的△H大于0 CO2(g)+H2(g)中的△H大于0 |
| B.图②是石墨为电极电解氯化钠稀溶液,阴、阳两极产生气体体积之比一定为1:1 |
| C.图③表示25℃,0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,pH随加入酸体积的变化 |
D.图④表示2SO2(g) + O2(g)  2SO3(g) ΔH < 0 正、逆反应平衡常数K随温度的变化 2SO3(g) ΔH < 0 正、逆反应平衡常数K随温度的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
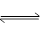 C(g)+D(g),
C(g)+D(g),查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 定不仅与焓变(ΔH)有关,也与温度(T)、熵变(ΔS)有关,实验证明,化学反应的方向应由ΔH-TΔS确定,若ΔH-TΔS<0则自发进行,否则不能自发进行。下列说法中不正确的是 ( )
定不仅与焓变(ΔH)有关,也与温度(T)、熵变(ΔS)有关,实验证明,化学反应的方向应由ΔH-TΔS确定,若ΔH-TΔS<0则自发进行,否则不能自发进行。下列说法中不正确的是 ( )A.在温度、压力一定的条件下,焓因素和熵因素共同决定一个化学 反应的方向 反应的方向 |
| B.温度、压力一定时,放热的熵增加反应一定能自发进行 |
| C.反应焓变是决定反应能否自发进行的唯一因素 |
| D.固体的溶解过程与熵变有关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放热反应一定是自发进行的反应 |
| B.化学反应的熵变与反应的方向无关 |
| C.焓变小于0而熵变大于0的反应肯定是自发的 |
| D.只有不需要任何条件就能够自动进行的过程才是自发过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
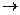 2C(g)+D(g)—Q当达到平衡后,在其
2C(g)+D(g)—Q当达到平衡后,在其| A.正反应速度增大,逆反应速度增大,平衡向正反应方向移动 |
| B.正反应速度增大,逆反应速度减小,平衡向正反应方向移动 |
| C.正反应速度增小,逆反应速度增大,平衡向逆反应方向移动 |
| D.正反应速度减大,逆反应速度增大,平衡向逆反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com