
����Ŀ�����淴Ӧ2NO2��g���T2NO��g��+O2��g�������������ܱ������з�Ӧ���������¼���˵����
����Ӧ������и����ʵ����ʵ���Ũ�����
����λʱ��������n mol O2 ��ͬʱ����2n mol NO2
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʱ�Ϊ2��2��1��״̬
������������ɫ���ٸı��״̬
�����������ܶȲ��ٸı��״̬
����������ƽ��Ħ���������ٸı��״̬
���б�ʾ��Ӧ�ﵽƽ��״̬����
A. �٢ۢ� B. �ڢܢ� C. �ڢۢܢ� D. �٢ڢܢ�
���𰸡�B
��������
���ݻ�ѧƽ��״̬��������𣬵���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ����Ҳ�������仯ʱ��һ���ﵽƽ��״̬��
�ٷ�Ӧ������и����ʵ����ʵ���Ũ����ȣ���һ���Dz��䣬���Բ�һ��ƽ�⣬�ʲ�ѡ�����ڵ�λʱ��������n mol O2��Ч������2n mol NO2ͬʱ����2n mol NO2�����淴Ӧ������ȣ�һ��ƽ�⣬��ѡ��������NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʱ�Ϊ2:2:1��״̬��һֱ���������ϵ����һ��ƽ�⣬�ʲ�ѡ�����ܻ���������ɫ���ٸı��״̬��˵������������Ũ�Ȳ��䣬��ѡ��;�ݻ��������ܶ�һֱ���䣬�����ܶȲ��䲻һ��ƽ�⣬�ʲ�ѡ��������![]() ��n�DZ��������Ի�������ƽ��Ħ�������DZ�����ƽ��Ħ���������ٸı��״̬һ����ƽ��״̬����ѡ�ޣ�ѡB��
��n�DZ��������Ի�������ƽ��Ħ�������DZ�����ƽ��Ħ���������ٸı��״̬һ����ƽ��״̬����ѡ�ޣ�ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������NO2����һ����Ҫ�Ĵ�����Ⱦ�������д�����
��1����������������ʱ������N2��O2��Ӧ����NO���䷴Ӧ�����е������仯���£�
��Ӧ | N2(g)��2N(g) | O2(g)��2O(g) | N(g)��O(g)��NO(g) |
��Ӧ�� | ��H1 | ��H2 | ��H3 |
����ֵkJ/mol | 945 | 498 | 630 |
�١�H1___0����H3____0��������>������<����
��N2��g��+O2��g��=2NO��g����H=____kJ��mol-1��
��2�����ü������ԭ���������֪��
CH4��g��+4NO2��g��==4NO��g��+CO2��g��+2H2O��g����H=-574kJ��mol-l
CH4��g��+4NO��g��==2N2��g��+CO2��g��+2H2O��g��AH=-1160 kJ��mol-l
H2O��l��=H2O��g����H=+44kJ��mol-l
CH4��NO2��Ӧ����N2��H2O(l)���Ȼ�ѧ����ʽΪ_______��
��3��DZͧ��ʹ�õ�Һ��-Һ��ȼ�ϵ�ع���ԭ����ͼ��ʾ��

���缫a������______��
���������Һ��OH-������_____�ƶ��������缫a�������缫b������
���缫b�ĵ缫��ӦʽΪ_____��
��4����ͨ��NH3��NaClO��Ӧ���Ƶû��ȼ���£�N2H4�����÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���![]() (I)��
(I)��![]() (II)��
(II)��![]() (III)��
(III)��![]() (IV)�������˵����ȷ����
(IV)�������˵����ȷ����
A. ���������������ķе��������� B. �������һ�ȴ����ֻ������
C. ��������̼ԭ�ӿ��ܶ�����ͬһƽ�� D. �����������ڷ����廯�����Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�������Һ������Ũ�ȹ�ϵʽ��ȷ����
A. pH=5��H2S��Һ�У�c(H+)= c(HS��)=1��10��5 mol��L��1
B. pH=a�İ�ˮ��Һ��ϡ��10������pH=b����a��b+1
C. pH=2��H2C2O4��Һ��pH=12��NaOH��Һ���������ϣ�c(Na��)+ c(H��)= c(OH��)+c( HC2O4��)+ c( C2O42-)
D. pH��ͬ�Ģ�CH3COONa��NaHCO3��NaClO������Һ��c(Na��)������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����20 mL0.5 molL��1K2SO3��Һ��μ��뵽20 mL 0.2 molL��1�����ữ����ɫKMnO4��Һ�У���Һǡ�ñ�Ϊ��ɫ����MnԪ���ڲ����еĴ�����̬�ǣ�������
A. Mn B. Mn2+ C. Mn2O3 D. K2MnO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ��������N2��H2��Ӧ�����������仯������ͼ������������ȷ����
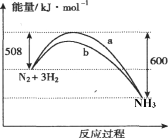
A. �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+3H2![]() 2NH3 ��H=��92kJ��mol��1
2NH3 ��H=��92kJ��mol��1
B. a�����Ǽ������ʱ�������仯����
C. ����������û�ѧ��Ӧ�ķ�Ӧ�Ƚ������ı�
D. ����ͬ�¶ȵ������£��������ͬI��II���������зֱ�ͨ��1mol N2��3 mol H2������I����㶨������II����ɱ䱣�ֺ�ѹ����Ӧ�������������ڵķ�Ӧ����v(I)��v(II)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
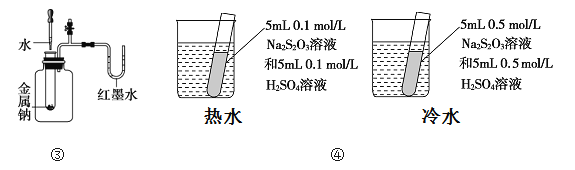
����Ŀ������װ�û�����ܴﵽĿ�ĵ���
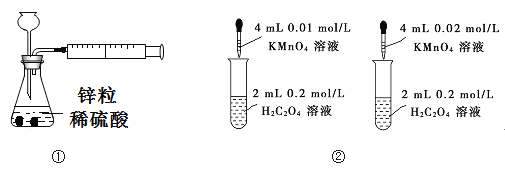
A. װ�������ڲⶨ��������������
B. װ����������ɫ�����Ƚ�Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
C. װ��������U������Һ��ĸߵ��ж�Na��ˮ��Ӧ����ЧӦ
D. װ�������ݳ��ֻ��ǵĿ����Ƚ��¶ȶԷ�Ӧ���ʵ�Ӱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ������λ����ͼ��ʾ����Yԭ�ӵ������������ڲ��������3��������˵����ȷ����
![]()
A. X����̬�⻯���Y���ȶ�
B. W������������Ӧˮ��������Ա�Z��ǿ
C. Z�ķǽ����Ա�Y��ǿ
D. X��Y�γɵĻ����ﶼ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.100 mol��L-1 AgNO3�ζ�50.0 mL 0.0500 mol��L-1 Cl-��Һ�ĵζ�������ͼ��ʾ�������й������������
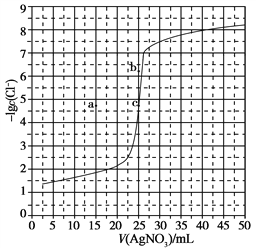
A. �����������ݼ����֪Ksp(AgCl)��������Ϊ10-10
B. �����ϸ������Һ�����ϵʽc(Ag+)��c(Cl-)=Ksp(AgCl)
C. ��ͬʵ�������£�����Ϊ0.0400 mol��L-1 Cl-����Ӧ�յ�c�Ƶ�a
D. ��ͬʵ�������£�����Ϊ0.0500 mol��L-1 Br-����Ӧ�յ�c��b�����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com