
| A. | CH2CH2--乙烯的结构简式 | B. | 乙醇的结构简式--C2H6O | ||
| C. | 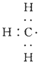 --甲基的电子式 --甲基的电子式 | D. | 四氯化碳的电子式为--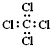 |
分析 A.乙烯的结构简式中没有标出其官能团碳碳双键;
B.乙醇的结构简式中需要标出其官能团羟基;
C.甲基中含有3个碳氢键,碳原子最外层为7个电子;
D.四氯化碳的电子式中,氯原子最外层达到8电子稳定结构,漏掉了氯原子的3对孤电子对.
解答 解:A.乙烯分子中含有碳碳双键,乙烯正确的结构简式为:CH2=CH2,故A错误;
B.乙醇分子中含有羟基,乙醇正确的结构简式为:C2H5OH,故B错误;
C.甲基为中性原子团,碳原子最外层为7个电子,甲基的电子式为: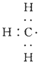 ,故C正确;
,故C正确;
D.四氯化碳中Cl原子周围8个电子,则四氯化碳正确的电子式为: ,故D错误;
,故D错误;
故选C.
点评 本题主要考查了最简式、结构简式、电子式、结构式等的书写,题目难度中等,试题侧重于基础知识的考查,注意含有官能团的有机物在书写结构简式时官能团不能缩写,D中注意明确甲烷与四氯化碳的电子式的区别,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | BeCl2 | C. | CO2 | D. | HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为锌、铜、硫酸铜溶液构成的原电池,请写出负极、以及电池总反应.
如图为锌、铜、硫酸铜溶液构成的原电池,请写出负极、以及电池总反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为 890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 500℃、30MPa 下,将 0.5mol N2(g)和 1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热 19.3 kJ,其热化学方程式为: N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | HCl 和 NaOH 反应的中和热△H=-57.3 kJ/mol,则 H2SO4 和 Ca(OH)2 反应的中和热△H=2×(-57.3)kJ/mol | |
| D. | 在 101 kPa 时,2gH2完全燃烧生成液态水,放出 285.8kJ 热量,氢气燃烧的热化学方程式表示为 2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-CH2-CH3与 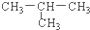 | B. | C3H8与C6H14 | ||
| C. | 乙烯和1,3-丁二烯 | D. | CH3CH2Cl 和CH2ClCH2CH2Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
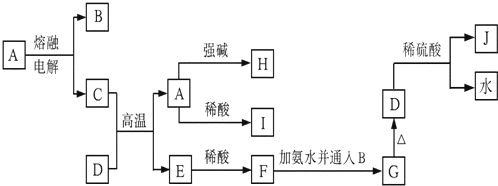
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径是第ⅡA族中最大的 | B. | 遇冷水能剧烈反应 | ||
| C. | 位于第七周期 | D. | Ra(OH)2是两性氢氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com