
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 地壳中含量最高的非金属元素 |
| Y | M层比K层多1个电子 |
| Z | 最外层电子数为内层电子数的0.6倍 |
| W | 与氯形成的氯化物是生活中常用的调味品 |
分析 X为地壳中含量最高的非金属元素,为O元素;Y的M层比K层多1个电子,为Al元素,Z的最外层电子数为内层电子数的0.6倍,为S元素;W与氯形成的氯化物是生活中常用的调味品,为Na元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答 解:X为地壳中含量最高的非金属元素,为O元素,Y的M层比K层多1个电子,为Al元素,Z的最外层电子数为内层电子数的0.6倍,为S元素,W与氯形成的氯化物是生活中常用的调味品,为Na元素,
(1)X为O,对应的双原子分子的结构式为O=O,对应的水中含有氢键,较一般的分子间作用力强,沸点较高,
故答案为:O=O;最高;水分子间存在氢键;
(2)Y为Al,工业用电解熔融的氧化铝冶炼,该电解的化学方程式为:2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,
故答案为:2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;
(3)Al单质与Na元素的最高价氧化物对应水化物恰好反应完全,生成NaAlO2,向反应后的溶液中通入过量的CO2,生成氢氧化铝和碳酸氢钠,发生反应的离子方程式为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,
故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(4)Z元素形成的强酸浓溶液为浓硫酸,铜与浓硫酸反应生成的气体为SO2,二氧化硫具有漂白性,可用品红溶液鉴别二氧化硫,
故答案为:SO2;品红溶液.
点评 本题考查了元素位置、结构和性质的关系,正确推断元素是解本题关键,结合元素在周期表中的位置、元素周期律来分析解答,注意相关化学方程式以及离子方程式的书写,题目难度中等.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 钙和磷都是人体内含量丰富的矿物元素,它们都属于微量元素 | |
| B. | 垃圾焚烧和发电技术的结合,既解决了污染问题,又有效利用了垃圾所含的能量 | |
| C. | 制造普通玻璃的主要反应原理之一为:CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$=CaSiO3 | |
| D. | 青霉素是最早发现的天然抗生素,其中起治疗作用的是水杨酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通过Na2O2使其增重28 g 时,反应中转移的电子数为0.5NA | |
| B. | 25℃时,Ksp(BaSO4)=1×10-10,则 Ba SO4饱和溶液中Ba2+数目为=1×10-5 NA | |
| C. | 标准状况下,22.4 L CH2Cl2中共价键的数目为4NA | |
| D. | 高温下,16.8g Fe与足量的水蒸气完全反应失去电子的数目为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加A 的量,平衡不移动 | |
| B. | 增加B 的量,平衡正向移动 | |
| C. | 升高体系温度,平衡常数K 增大 | |
| D. | 压缩气体体积,正、逆反应速率均增大,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:l | B. | 1:3 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.01 mol•L-1的碳酸钠溶液 | B. | pH=12的Ba(OH)2溶液中 | ||
| C. | 0.01 mol•L-1的醋酸 | D. | 0.01 mol•L-1的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(SO3 )=v(NO2) | |
| B. | 混合气体的密度保持不变 | |
| C. | 混合气体的颜色保持不变 | |
| D. | 每消耗1 mol SO3的同时生成1 mol NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
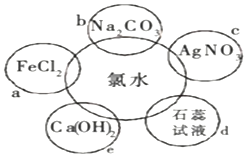 完成下列题目
完成下列题目查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com