
电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s) +4HCl(aq) 2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
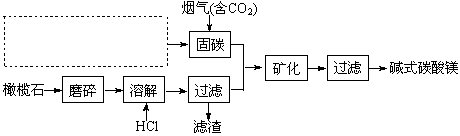
(1)某橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 。
 (2)固碳时主要反应的方程式为NaOH(aq)+CO2 (g)=NaHCO3 (aq),该反应能自发进行的原因是 。
(2)固碳时主要反应的方程式为NaOH(aq)+CO2 (g)=NaHCO3 (aq),该反应能自发进行的原因是 。
(3)请在上图虚框内补充一步工业生产流程
。
(4)下列物质中也可用作“固碳”的是 。
(填字母)
a.CaCl2 b.H2NCH2COONa c.(NH4)2CO3
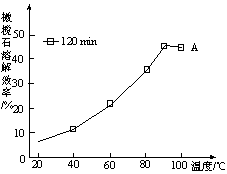
(5)由图可知,90℃后曲线A溶解效率下降,分
析其原因 。
(6)经分析,所得碱式碳酸镁产品中含有少量NaCl和Fe2O3。为提纯,可采取的措施依次为:对溶解后所得溶液进行除铁处理、对产品进行洗涤处理。判断产品洗净的操作是 。
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
关于酸、碱、盐的下列各种说法中,正确的是( )
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,只生成金属阳离子和酸根阴离子的是盐
D.NH4Cl的电离方程式是:NH4Cl===NH4++Cl-,所以NH4Cl是盐
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.SO2能使品红溶液、溴水和酸性:KMnO4溶液褪色,是因为SO2具有漂白性
B.SO2、Cl2都可用于漂白物质,将等物质的量的两种气体同时作用于潮湿的有色物质时,可增强漂白效果
C.活性炭使有色物质褪色是利用了碳单质的还原性,使有色物质发生了还原反应
D.SO2使品红溶液褪色后,将褪色后的溶液加热,溶液重新变为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
| ② | ③ | ④ | ||
| 甲 | C | N2 | S | Fe |
| 丙 | CO2 | NO2 | SO3 | Fe(NO3)3 |
甲、乙、丙、丁四种物质,甲、乙、丙含同一种元素。下列各组物质可按下图转化的是
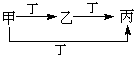
A.①② B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.准确称取0.4000 g NaOH固体可配成100 mL 0.1000 mol·L-1的NaOH标准溶液
B.已知Ksp[Fe(OH)3]=4.0×10-38,则Fe3++3H2O Fe(OH)3+3H+的平衡常数K=2.5×10-5
Fe(OH)3+3H+的平衡常数K=2.5×10-5
C.100 mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱
D.对于反应2SO2(g)+O2(g) 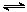 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
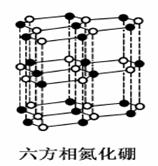
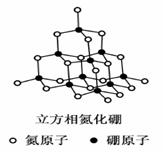
(1)基态硼原子的电子排布式为 。
(2)关于这两种晶体的说法,正确的是 (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石墨相似却不导电,原因是 。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为 。该晶体的天然矿物在青藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有 mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有几种物质,请按要求回答问题。
①食盐与沙子 ②从NaCl溶液中获得晶体
③水和汽油的混合物 ④用CCl4提取碘水中的碘
(1)分离①、②的操作分别为___________、___________。
(2)③和④共同使用的仪器且在其他组分分离时无需使用,这种仪器是_______。
(3)上述需使用酒精灯的是________(填序号)。
(4)从碘的四氯化碳溶液中得到纯净的碘的方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学研究铝及其化合物的性质时设计了如下两个实验方案。
方案一:2.7 g Al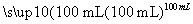 X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀
方案二:2.7 g Al Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀
已知:NaOH溶液和稀盐酸的浓度均是3 mol·L-1,如图是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
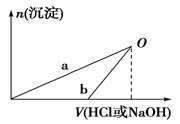
A.在O点时两方案中所得溶液的溶质物质的量相等
B.b曲线表示的是向X溶液中加入NaOH溶液
C.X溶液溶质为AlCl3,Y溶液溶质为NaAlO2
D.a、b曲线表示的反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如图所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气。过一段时间后可观察到______________,发生反应的化学方程式为______________________________________________________。
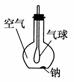
(2)某班同学用如图所示装置测定空气里氧气的含量。先用弹簧夹夹住橡胶管。点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。

①上述实验过程中发生反应的化学方程式为:
________________________________________________________________________。
②实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是________。
a.甲同学可能使用钠的量不足,瓶内氧气没有消耗完
b.甲同学可能未塞紧瓶塞,钠熄灭冷却时外界空气进入瓶内
c.乙同学可能没夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出
d.乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com