
| A. | 3.0g | B. | 6.0g | C. | 9.0g | D. | 18.0g |
分析 根据n=$\frac{m}{M}$计算出二氧化硫的物质的量,然后可计算出该二氧化硫中含有的原子数,再结合NO的分子组成计算出一氧化氮的物质的量,最后根据m=nM计算出需要NO的质量.
解答 解:12.8gSO2的物质的量为:$\frac{12.8g}{64g/mol}$=0.2mol,0.2mol SO2中含有原子的物质的量为:0.2mol×3=0.6mol,
含有0.6mol原子需要NO的物质的量为:$\frac{0.6mol}{2}$=0.3mol,需要NO的物质的量为:30g/mol×0.3mol=9.0g,
故选C.
点评 本题考查了物质的量的简单计算,题目难度不大,明确物质的量与其它物理量之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的化学计算能力.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol•L-1的Ca(ClO)2溶液中含ClO-数目为NA | |
| B. | 标准状况下,22.4L水中含有的分子数为NA | |
| C. | 92g NO2和N2O4混合气体中含有的原子数为6NA | |
| D. | 1.7g H2O2中含有的电子数为0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
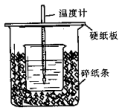 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z | |
| B. | X、Y 均能与W形成的离子化合物 | |
| C. | Z、W的气态氢化物的稳定性:Z>W | |
| D. | X、Z的最高价氧化物的水化物酸性:X>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16:25 | B. | 1:7 | C. | 1:6 | D. | 2:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com