
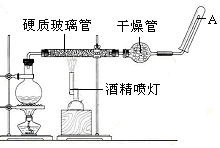
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.分析 (1)铁与水蒸气发生氧化还原反应,生成四氧化三铁和氢气,据此书写化学方程式;
(2)根据冒出的气泡和回流的水柱来判断;
(3)放置了几片碎瓷片防止暴沸;
(4)如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;该装置先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯,防止先点燃酒精喷灯导致Fe与O2的反应.
解答 解:(1)铁和水蒸气反应,铁的化合价升高,铁作还原剂,水中氢的化合价降低,水作氧化剂,反应的化学方程式为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(2)检查装置气密性的方法是:把导管口的下端浸入水中,用双手紧握烧瓶的外壁,如果观察到导管口有气泡冒出,且松手后导管内形成一段水柱,则气密性良好.故答案为:把导管口的下端浸入水中,用双手紧握烧瓶的外壁,如果观察到导管口有气泡冒出,且松手后导管内形成一段水柱,则气密性良好;
(3)因为反应物为水蒸气与铁,所以这里加热的目的就是提供水蒸气,烧瓶底部应事先放置碎瓷片,放碎瓷片的目的是防止沸腾事故发生,
故答案为:提供反应的水蒸气; 防止爆沸;
(4)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,产生水蒸气后,排掉硬质玻璃管内空气,再点燃酒精喷灯,
故答案为:先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯;防止先点燃酒精喷灯导致Fe与O2的反应.
点评 本题以铁与水的反应考查氧化还原反应,明确物质的性质及反应中元素的化合价变化即可解答,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 室温下用广范pH试纸测得某氯水的pH=4 | |
| B. | 将稀氯化铁溶液和稀硫氰化钾溶液混合,溶液呈浅红色,无论向其中加入浓氯化铁溶液还是浓硫氰化钾溶液,红色都会加深 | |
| C. | 用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,滴定前仰视读数,滴定后俯视读数会导致待测碱液浓度结果偏高 | |
| D. | 实验测定酸碱滴定曲线时,要保证整个过程测试和记录pH的间隔相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2 g O2含有的分子数为0.5NA | |
| B. | 71 g Cl2所含原子数为2NA | |
| C. | 标准状况下,22.4 L H2O含有的分子数为1NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeCl3与沸水反应生成NA个Fe(OH)3胶粒 | |
| B. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA | |
| C. | 25℃,1.01×105Pa,11.2L Cl2含有的分子数小于0.5NA | |
| D. | 常温下,23 g NO2含有2NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 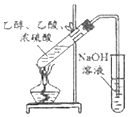 实验室中制取少量的乙酸乙酯 | B. | 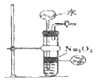 制备少量氧气 | ||
| C. |  验证NaHCO3和Na2CO3的热稳定性 | D. | 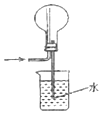 氯化氢气体的吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com