
将a g CuO和Fe2O3的混合物分成两等份,向其中一份中加入b mL c mol/L的稀盐酸正好完全反应;另一份在加热的条件下用H2还原,反应完全时用去H2 d L(折算成标准状况)。则 d 等于( )
A.11.2 bc×10-3
B.22.4 bc×10-3
C.22.4 (3a-4bc×10-3)
D.22.4 (3a-4bc)×10-3
科目:高中化学 来源: 题型:阅读理解
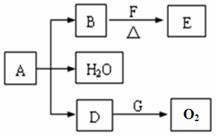
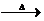 CH3CHO+H2O+Cu
CH3CHO+H2O+Cu CH3CHO+H2O+Cu
CH3CHO+H2O+Cu
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 11a |
| 36 |
| 11a |
| 20 |
| 11a |
| 36 |
| 11a |
| 20 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
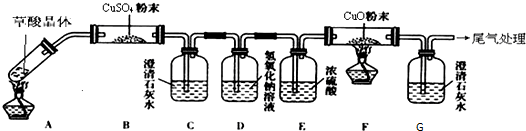
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北荆门高二上学期期末教学质量检测化学试卷(带解析) 题型:填空题
工业上通常在恒容密闭容器中采用CO(g)和H2 (g)反应催化合成甲醇CH3OH(g):
(1)已知:① 2CO(g) + O2 (g) = 2CO2 (g) ΔH =" -566.0" kJ·mol-1
② 2H2(g) + O2 (g) ="2" H2O (g) ΔH =" -398.0" kJ·mol-1
③2CH3OH(g) +3O2 (g) =2CO2 (g) +4 H2O(g) ΔH =" -1104.0" kJ·mol-1
则CO(g)与H2(g)合成CH3OH(g)的热化学方程式是_______________。
(2)据研究,反应过程中起催化作用的为CuO,反应体系中含少量CO2有利于维持催化剂CuO的量不变,原因是:_______________________________ (用化学方程式表示)。
(3)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
A. 混合气体的密度不变
B. 混合气体的平均相对分子质量不变
C. CH3OH(g)、CO(g)、H2(g)的浓度都不再发生变化
D.生成CH3OH(g)的速率与消耗CO(g)的速率相等
(4)下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.250 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡数据 | CH3OH的浓度(mol/L) | c 1 | c 2 | c 3 |
| 反应的能量变化的绝对值(kJ) | a | b | c | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源:2014届湖北荆门高二上学期期末教学质量检测化学试卷(解析版) 题型:填空题
工业上通常在恒容密闭容器中采用CO(g)和H2 (g)反应催化合成甲醇CH3OH(g):
(1)已知:① 2CO(g) + O2 (g) = 2CO2 (g) ΔH =" -566.0" kJ·mol-1
② 2H2(g) + O2 (g) ="2" H2O (g) ΔH =" -398.0" kJ·mol-1
③2CH3OH(g) +3O2 (g) =2CO2 (g) +4 H2O(g) ΔH =" -1104.0" kJ·mol-1
则CO(g)与H2(g)合成CH3OH(g)的热化学方程式是_______________。
(2)据研究,反应过程中起催化作用的为CuO,反应体系中含少量CO2有利于维持催化剂CuO的量不变,原因是:_______________________________ (用化学方程式表示)。
(3)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
A. 混合气体的密度不变
B. 混合气体的平均相对分子质量不变
C. CH3OH(g)、CO(g)、H2(g)的浓度都不再发生变化
D.生成CH3OH(g)的速率与消耗CO(g)的速率相等
(4)下表所列数据是反应在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.250 |
0.012 |
某温度下,将2molCO(g)和6mol H2(g)充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.5mol/L,则CO(g)的转化率为________,此时的温度为__________。
(5)要提高CO(g)的转化率,可以采取的措施是__________。
A. 升高温度 B. 加入催化剂 C. 增加CO(g)的浓度
D. 加入H2(g)加压 E. 分离出甲醇 F.加入惰性气体加压
(6)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
|
容器 |
甲 |
乙 |
丙 |
|
|
反应物投入量 |
1molCO 2molH2 |
1molCH3OH |
2molCH3OH |
|
|
平衡数据 |
CH3OH的浓度(mol/L) |
c 1 |
c 2 |
c 3 |
|
反应的能量变化的绝对值(kJ) |
a |
b |
c |
|
|
体系压强(Pa) |
P1 |
P2 |
P3 |
|
|
反应物转化率 |
α1 |
α2 |
α3 |
下列说法正确的是__________。
A. 2c1>c3 B. a+b=129 C. 2p2<p3 D. α1+α3<1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com