
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
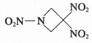
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.微粒半径:S﹥S2―﹥Cl―﹥F | B.酸性:HClO4﹥H2SO4﹥H3PO4 |
| C.氧化性:Cl2﹥S﹥Se﹥Te | D.离子还原性:S2―﹥I―﹥Br―﹥OH― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.W元素的单质属于原子晶体。 |
| B.X元素的非金属性比Y元素非金属性强 |
| C.Z和X能以共价键结合形成一种无机非金属材料 |
| D.Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
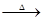 Z+W
Z+W
 混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)
混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com