
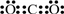 ����
����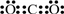 ��CO2�ĽṹʽΪO=C=O���ʴ�Ϊ��O=C=O��
��CO2�ĽṹʽΪO=C=O���ʴ�Ϊ��O=C=O��
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ը��������Һ | B����ˮ |
| C������ | D��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
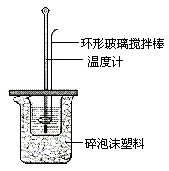 ��֪�ⶨ�к��ȵ�ʵ�鲽�����£�����ȡ30mL 0.5mol/L���ᵹ��С�ձ��У������¶ȣ� ����ȡ50mL 0.5mol/L NaOH��Һ�������¶ȣ� �۽�NaOH��Һ����С�ձ��У���Ͼ��Ⱥ�������Һ�¶ȣ��ش���������
��֪�ⶨ�к��ȵ�ʵ�鲽�����£�����ȡ30mL 0.5mol/L���ᵹ��С�ձ��У������¶ȣ� ����ȡ50mL 0.5mol/L NaOH��Һ�������¶ȣ� �۽�NaOH��Һ����С�ձ��У���Ͼ��Ⱥ�������Һ�¶ȣ��ش����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3��Һ�У�c��OH-��-c��H+��=c��HCO3-��+2c��H2CO3�� |
| B��NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
| C��pH=2��������pH=12�İ�ˮ������������������Һ�У�c��H+��+c��NH4+��=c��OH-��+c��Cl-�� |
| D�������ʵ���Ũ�ȵ�CH3COOH��CH3COONa��Һ�������Ϻ�������Һ�У�c��CH3COO-��+2c��OH-��=2c��H+��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com