
(15分)某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去)。
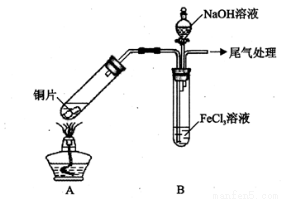
(1)实验前,应先检查装置的 ;实验中产生的尾气应通人 溶液。
(2)实验过程中需要配制100mL1mol/L FeCl3溶液(未用浓盐酸酸化),所需要的玻璃仪器有:烧杯、量筒、玻璃棒、 。
(3)该小组同学向5mL lmol/L FeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是 。
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色。
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO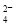 。
。
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
(5)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了如下实验:

向步骤①和步骤②所得溶液中加入某种试剂,溶液立即出现蓝色沉淀,则该试剂中含有溶质的化学式是 。
(6)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ. 。
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:填空题
(6分)已知下列热化学方程式:
①H2(g)+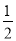 O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+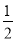 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+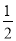 O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)表示C的燃烧热的热化学方程式为________;(填序号)
(2)燃烧10 g H2生成液态水,放出的热量为________。
(3)写出表示CO的燃烧热的热化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河东区高三一模理综化学试卷(解析版) 题型:选择题
下表是在相同温度下,三种酸的一些数据,下列说法正确的是
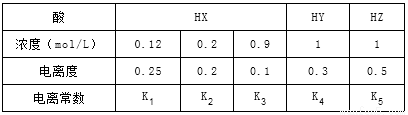
A.相同温度下,从HX的数据可以说明:弱电解质溶液浓度越低,电离度越大,且K1>K2>K3=0.1
B.室温时,若在NaZ溶液中加水,则c(Z-)/[c(HZ)×c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-)
D.相同温度下,K5>K4>K3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:推断题
(16分)有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
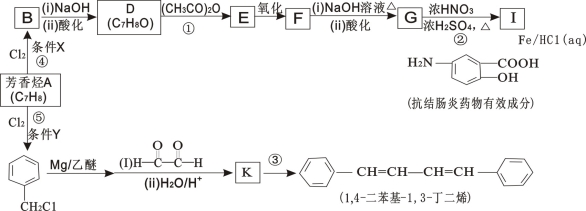
已知:
Ⅰ.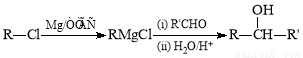 (R、R`表示烃基)
(R、R`表示烃基)
Ⅱ.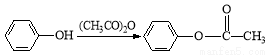
Ⅲ.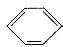
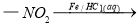

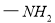
Ⅳ.

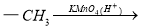

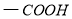
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是 。
(2)D的结构简式是_______________
(3)写出F与NaOH反应的化学方程式 。
(4)下列说法正确的是________(填选项字母)。
A.④的反应条件X和⑤的反应条件Y完全相同
B.①②④⑤反应类型相同
C.G不可以发生缩聚反应
D.设计D→E和F→G两步反应的目的是防止酚羟基被氧化
(5)检验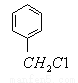 有氯原子的方法是 。
有氯原子的方法是 。
(6)③的化学方程式是 。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式: 。
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
c.其核磁共振氢谱有3种峰,峰面积之比为3∶2∶2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:选择题
能正确表示下列反应离子方程式的是
A.向NaAlO2溶液中通入过量CO2制Al(OH)3:2AlO2-+CO2+3H2O= 2Al(OH)3↓+ CO32-
B.双氧水中加入稀硫酸和KI溶液:2I﹣+H2O2+2H+=I2+O2↑+2H2O
C.Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+ BaSO4↓
D.草酸使酸性KMnO4溶液褪色,其离子方程式为:5H2C2O4 + 2MnO4-+ 6H+ = 2Mn2+ + 10CO2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三“二诊”考试化学试卷(解析版) 题型:选择题
下列有关实验操作设计、现象记录、结论解释都正确的是
实验操作设计 | 现象记录 | 结论解释 | |
A | 将少量浓硝酸逐滴加入Cu和稀硫酸的混合物中 | 产生红棕色气体 | 硝酸被还原为NO2 |
B | 用坩埚钳夹住铝箔在酒精灯上加热 | 铝箔熔化但并不滴落 | 熔点:Al2 O3>Al |
C | 向某氯化亚铁溶液中加入 Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化 亚铁溶液已经变质 |
D | 向紫色石蕊试液中持续长时间通人氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
(19分)某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。
查阅资料:Cu2O在酸性溶液中会发生反应: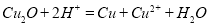
探究一:用下图所示装置进行实验,回答下列问题:

(1)仪器组装完成后,夹好止水夹,__________.则说明装置A的气密性良好。
(2)装置A是氢气的发生装置,可以选用的药品是_________(填选项)
A.稀硫酸和锌片 B.稀硝酸和铁片
C.氢氧化钠溶液和铝片 D.浓硫酸和镁片
(3)从下列实验步骤中,选择正确的操作顺序:①________③(填序号)
①打开止水夹
②熄灭C处的酒精喷灯
③C处冷却至室温后,关闭止水夹
④点燃C处的酒精喷灯
⑤收集氢气并验纯
⑥通入气体一段时间,排尽装置内的空气
(4)收集氢气验纯时,最好采用___________方法收集氢气。
探究二:
(5)取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;此观点是否正确_________。(填“是”或“否”)若填“否”,则原因是_________(用离子方程式说明);另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体。
证明样品中一定含有__________,取少量反应后的溶液,加适量蒸馏水稀释后,滴加_________(填试剂和实验现象),则可证明另一成分存在,反之,说明样品中不含该成分。
探究三:
(6)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中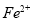 有1.0mol,则样品中
有1.0mol,则样品中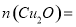 ___________mol。
___________mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:选择题
在下列各反应的离子方程式书写中,正确的是
A.将Na2O2放入水中发生的反应:Na2O2+2H2O=2Na++2OH-+O2↑
B.除去CuSO4溶液中的Fe3+:2 Fe3++3Cu=2Fe+3Cu2+
C.在KOH溶液中,甲烷-氧气燃料电池放电时的反应:CH4+2O2+2OH-=CO32-+ 3H2O
D.电解饱和食盐水制备H2和Cl2:2Cl-+2H+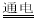 Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三下学期第一次模考理综化学试卷(解析版) 题型:选择题
已知:2Fe+3Cl2 2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
A.氯气是氧化剂,FeCl3是还原剂
B.常温下,与56g Fe反应断裂1.5NA个Cl-Cl键
C.1 L 0.1 mol·L-1 FeCl3溶液中含有0.1NA个Fe3+
D.常温常压下,22.4 L Cl2和足量Fe反应转移3NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com