
| A. | 上述实验条件下,物质的氧化性:Cu>SO2>I2 | |
| B. | 在SO2与I2反应中得到的还原产物为H2SO4 | |
| C. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 | |
| D. | 滴加KI溶液时.每转移2mole-会生成2molCuI沉淀 |
分析 溶液呈棕色,说明有I2生成.碘元素化合价由-1价升高到0价,硫酸根只有在浓硫酸中有氧化性,所以化合价能够降低的只有Cu2+,观察到产生白色沉淀,由于Cu为红色,所以Cu2+不能还原为Cu,应还原为Cu+.向反应后的混合物中不断通入SO2气体,并加热,溶液逐渐变成无色,说明I2反应,发现白色沉淀显著增多,故I2与SO2反应生成I-,SO2被氧为化H2SO4,白色沉淀是CuI,据此分析.
解答 解:CuSO4溶液中逐滴加入KI溶液化学方程式为2CuSO4+4KI═2K2SO4+2CuI↓+I2,向反应后的混合物中不断通入SO2气体,反应方程式:SO2+2H2O+I2=H2SO4+2HI.
A.2CuSO4+4KI═2K2SO4+2CuI↓+I2反应中Cu2+化合价降低是氧化剂,I2是氧化产物,氧化剂的氧化性强于氧化产物的氧化性,所以物质的氧化性:Cu2+>I2,SO2+2H2O+I2=H2SO4+2HI中碘元素化合价由0价降低为-1价,I2是氧化剂,SO2被氧化,所以物质氧化性I2>SO2,所以氧化性Cu2+>I2>SO2,Cu没有氧化性,故A错误;
B.反应后的混合物中不断通入SO2气体,反应方程式:SO2+2H2O+I2=H2SO4+2HI,由反应可知,碘元素化合价由0价降低为-1价,被还原,所以还原产物为HI,故B错误;
C.向反应后的混合物中不断通入SO2气体,反应方程式:SO2+2H2O+I2=H2SO4+2HI,因为发生氧化还原反应使碘褪色,二氧化硫不表现漂白性,故C错误;
D.CuSO4溶液中逐滴加入KI溶液化学方程式为2CuSO4+4KI═2K2SO4+2CuI↓+I2,由方程式可知每转移2mol电子生成2molCuI,故D正确.
故选:D.
点评 本题考查氧化还原反应,根据题目信息推断实验中发生的反应,素材陌生,难度中等,注意从化合价的角度分析氧化还原反应,考查学生的分析能力和对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 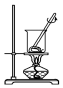 灼烧海带 | B. | 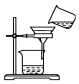 过滤得含I-的溶液 | ||
| C. | 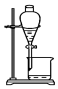 放出碘的苯溶液 | D. | 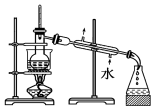 分离碘并回收苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅与NaOH溶液反应:SiO2+2OH-═SiO32-+H2O | |
| B. | 碳酸钡溶于稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 氯气与NaOH溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 把水玻璃滴入盐酸中:SiO32-+2H+═H2SiO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸和碱反应只能生成盐和水 | |
| B. | ${\;}_{7}^{14}$N+${\;}_{0}^{1}$n→${\;}_{6}^{12}$C+${\;}_{1}^{3}$H,此过程为化学变化 | |
| C. | 金属主要发生吸氧腐蚀,其本质是被氧化 | |
| D. | Na2O2的水溶液能导电,所以Na2O2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤炭经气化、液化和干馏等过程,可以转化为淸洁能源 | |
| B. | 利用二氧化碳来制造全降解塑料,可以缓解温室效应 | |
| C. | 高纯硅可用于制造太阳能电池、计算机芯片和光异纤维 | |
| D. | 在医疗上.可用碳酸氢钠治疗胃酸过多症 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
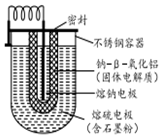
| A. | 熔钠电极作电池的正极 | |
| B. | 放电时Na+向正极移动 | |
| C. | 充电时熔钠电极与电源的正极相连 | |
| D. | 充电时阳极反应式为8Sn2--16e-=nS8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解Na C l溶液制备Cl2:2C1-+2H2O$\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- | |
| B. | 向MgCl2溶液中加入氨水制备Mg(OH)2:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 将Fe S溶于稀硝酸制备Fe(NO3)3:FeS+4 H++NO3═Fe3++NO↑+S↓+2H2O | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2 MnO4-+6 H++5 H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com