
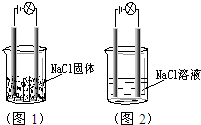
 一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接 好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | |
| B. | 将图2中的NaCl溶液换成液态HCl,灯泡也亮 | |
| C. | 将图2中的NaCl溶液换成SO2的水溶液,灯泡也亮,说明SO2是电解质 | |
| D. | 电解质本身不一定能导电 |
分析 根据原电池的工作原理和构成条件:电解质溶液必须含有大量自由移动离子,电解质中阴阳离子的定向移动形成电流.而电解质是在水溶液中或熔融状态下本身能电离出自由移动的离子而导电的化合物,据此分析.
解答 解:A、NaCl是强电解质,故A错误;
B、液态HCl是共价化合物,在水溶液中才能电离出自由移动的离子而导电,液态时不电离,故不导电,故换成液态的HCl,灯泡不亮,故B错误;
C、SO2的水溶液能导电,是由于二氧化硫溶于水生成了H2SO3能电离的出自由移动离子的原因,与SO2本身无关,而液态的SO2又不导电,故SO2是非电解质,故C错误;
D、NaCl是电解质,但其在固态时不导电,故电解质本身不一定能导电,故D正确.
故选D.
点评 本题考查学生电解池的构成条件中的:含有电解质溶液或是熔融的电解质这一条知识,注意知识的迁移应用能力的培养是关键,难度中等.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 正极为Cu、负极为Fe,电解质溶液为FeCl3溶液 | |
| B. | 正极为C、负极为Fe,电解质溶液为H2SO4溶液 | |
| C. | 正极为Ag、负极为Fe,电解质溶液为FeSO4溶液 | |
| D. | 正极为Ag、负极为Fe,电解质溶液为Fe2(SO4)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用25mL碱式滴定管准确量取22.00 mL的KMnO4溶液 | |
| B. | 用托盘天平准确称取9.8g NaCl 固体 | |
| C. | 用广泛pH试纸测出某盐酸溶液的pH为3.2 | |
| D. | 用10mL量筒量取7.50mL稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+=Fe2++Cu | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与盐酸反应:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com