
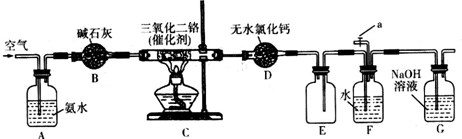
分析 A中通入空气,提供氧气,并将氨气鼓入C中,B装置干燥混合气体,C装置中发生氨的催化氧化生成NO,未反应的氨气可以在D中被氯化钙吸收,再装置E中NO进一步被氧气氧化生成二氧化氮,装置F中二氧化氮与水反应生成硝酸,反应会导致装置内压强降低,装置E具有防倒吸作用,用氢氧化钠溶液吸收氮的氧化物,防止污染空气.
(3)为充分利用NO,应打开活塞a,通入空气;若实验过程中观察到F中产生白烟,应有氨气存在,与硝酸反应生成硝酸铵,鼓入空气速度过快、氨水浓度过高都会导致氯化钙不能完全吸收氨气;
(4)根据c=$\frac{1000ρw}{M}$计算NaOH溶液物质的量浓度;
a.NaOH固体易潮解,具有腐蚀性,应放在小烧杯中称量;
b.固体NaOH溶解放出大量的热,应冷却室温后再移入容量瓶中;
c.定容时,当液面离容量瓶颈部的刻度线下l-2cm时,改用胶头滴管向容量瓶中滴加蒸馏水至凹液面的最低处恰好与刻度线相切;
d.少量溶液残留在瓶塞与瓶口之间,不需要加水;
(5)根据电子转移守恒计算氨气与NOx恰好反应的体积比,实际体积之比应大于或等于该值,保证氮的氧化物完全反应.
解答 解:A中通入空气,提供氧气,并将氨气鼓入C中,B装置干燥混合气体,C装置中发生氨的催化氧化生成NO,未反应的氨气可以在D中被氯化钙吸收,再装置E中NO进一步被氧气氧化生成二氧化氮,装置F中二氧化氮与水反应生成硝酸,反应会导致装置内压强降低,装置E具有防倒吸作用,用氢氧化钠溶液吸收氮的氧化物,防止污染空气.
(1)装置B的作用是:吸收气体中水蒸气,装置C玻璃管中发生反应的化学方程式为:4NH3+5O2$\frac{\underline{\;三氧化二铬\;}}{△}$4NO+6H2O,
故答案为:吸收气体中水蒸气;4NH3+5O2$\frac{\underline{\;三氧化二铬\;}}{△}$4NO+6H2O;
(2)装置E有两个作用,一是使NO进一步氧化;二是防止倒吸,故答案为:防止倒吸;
(3)装置F中,发生反应的离子方程式为:3NO2+H2O=2H++2NO3-+NO;为充分利用NO,应打开活塞a,缓缓通入适量空气;若实验过程中观察到F中产生白烟,应有氨气存在,与硝酸反应生成硝酸铵,鼓入空气速度过快、氨水浓度过高都会导致氯化钙不能完全吸收氨气,
故答案为:3NO2+H2O=2H++2NO3-+NO;打开活塞a,缓缓通入适量空气;ab;
(4)根据c=$\frac{1000ρw}{M}$可知,NaOH溶液物质的量浓度为$\frac{1000×1.2×10%}{40}$mol/L=3mol/L;
a.NaOH固体易潮解,具有腐蚀性,应放在小烧杯中称量,故a正确;
b.固体NaOH溶解放出大量的热,应用液体有热胀冷缩吸收,未冷却直接引入容量瓶,恢复室温会导致溶液体积偏小,应冷却室温后再移入容量瓶中,故b错误;
c.定容时,当液面离容量瓶颈部的刻度线下l-2cm时,改用胶头滴管向容量瓶中滴加蒸馏水至凹液面的最低处恰好与刻度线相切,故c正确;
d.少量溶液残留在瓶塞与瓶口之间,不影响溶液浓度,若再加水至刻度线,会导致溶液浓度偏低,故d错误,
故答案为:3mol/L;ac;
(5)x=1.5时,NOx中N原子平均化合价为+3,二者恰好反应时,根据电子转移守恒:n(NH3)×3=n(NOx)×3,故n(NH3):n(NOx)=1,氮的氧化物完全反应,故相同条件下$\frac{V(N{H}_{3})}{V(N{O}_{x})}$≥1,
故答案为:1.
点评 本题考查实验制备、物质的量浓度计算、溶液配制、氧化还原反应计等,实验拼合型题目,明确结合反应原理明确各装置的作用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 通氧气的电极为阳极,发生氧化反应 | |
| B. | 电池放电时,外电路电子由通氧气的正极流向通氢气的负极 | |
| C. | 正极的电极反应为:4OH-→O2↑+2H2O+2e- | |
| D. | 电池工作时,CO${\;}_{3}^{2-}$向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
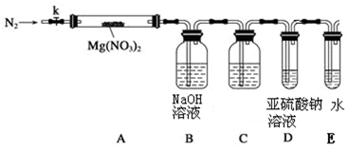 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2a | B. | 2a+2 | C. | 2a+10 | D. | a+2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 | |
| B. | 石油干馏可得到石油气、汽油、煤油、柴油等 | |
| C. | 变质的油脂有特殊难闻气味,是因为油脂发生了氧化反应 | |
| D. | 制作快餐盒的聚苯乙烯塑料是易降解塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
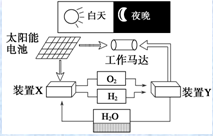
| A. | 装置X能实现燃料电池的燃料和氧化剂再生 | |
| B. | 装置Y中负极的电极反应式为O2+2H2O+4e-═4OH- | |
| C. | 该系统中只存在3种形式的能量转化 | |
| D. | 装置X、Y形成的子系统能实现物质零排放,并能实现化学能与电能间的完全转化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com