
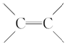 )不能自由旋转,因此
)不能自由旋转,因此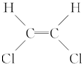 和
和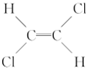 是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )
是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )| A. | 12种 | B. | 11种 | C. | 9种 | D. | 10种 |
分析 据官能团位置异构首先写出C3H4Cl2的同分异构体,然后确定哪些同分异构体还存在顺反异构,据此判断即可.
解答 解:C4H7Cl的同分异构体存在5种,即:CHCl=CH-CH2-CH3、CH2=CCl-CH2-CH3、CH2=CH-CH2Cl-CH3、CH2=CH-CH2-CH2Cl、CH2Cl-CH=CH-CH3、CH3-CHCl=CH-CH3、CHCl=C(CH3)、CH2=C(CH2Cl)CH3,共8种,其中只有双键碳中同碳上连接的基团不同时才具有顺反异构,故CHCl=CH-CH2-CH3、CH2Cl-CH=CH-CH3、CH3-CHCl=CH-CH3均存在顺反异构体,增加3种,即8+3=11种,故选B.
点评 本题主要考查同分异构体的书写,题目难度不大,注意根据等效氢原子判断一氯代物的个数是解决本题的关键.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.
A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 | |
| C. | 铵盐受热易分解,因此贮存氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 不能用稀HNO3和金属反应制取氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
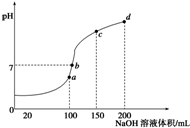 常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是( )
常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是( )| A. | a、b、c、d四个点中,水的电离程度最大的是d | |
| B. | a点溶液中:c(NH3•H2O)+c(H+)═c(OH-) | |
| C. | b点溶液中:c(Na+)+c(NH4+)═2c(SO42-) | |
| D. | c点溶液中:c(Na+)═c(SO42-)+c(NH4+)+c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:
在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:| A. | 在T2时,若反应体系处于状态D,则此时v正>v逆 | |
| B. | 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 若状态B、C、D的压强分别为PB、PC、PD,则 PC=PD>PB | |
| D. | 该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,向 0.1mol•L-1CH3COOH 溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中的$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$值减小到原来的$\frac{1}{10}$ | |
| B. | 常温时,将PH=1的醋酸和 PH=13的NaOH溶液等体积混合后的溶液:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| C. | 常温下0.1mol•L-1的下列溶液①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③ | |
| D. | 室温下,将0.4mol/LHA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化)测得混合液pH=5,则c(A-)+c(OH- )>c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
| pH | 7.5 | 11.6 | 9.7 | 8.3 |
| A. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF | |
| B. | 等体积等物质的量浓度的NaClO溶液与NaF溶液中离子总数大小:N前<N后 | |
| C. | 若将CO2通入0.1mol/L Na2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)═0.1mol/L | |
| D. | 向Na2CO3溶液中通入少量的HF气体,化学反应方程式为:Na2CO3+2HF═CO2+H2O+2NaF |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com