
下列叙述中正确的是( )
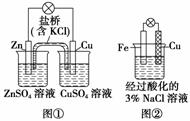
A.图①中正极附近溶液pH减小
B.图①中电子由Zn流向Cu,盐桥中的Cl-移向CuSO4溶液
C.图②正极反应是O2+2H2O+4e-===4OH-
D.图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.油脂的皂化反应生成脂肪酸和丙醇(2013·广东理综,7C)
B.蛋白质的水解产物都含有羧基和羟基(2013·广东理综,7D)
C.纤维素和淀粉遇碘水均显蓝色(2011·广东理综,7A)
D.淀粉、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
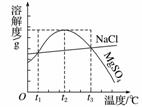
右图是NaCl、MgSO4的溶解度曲线。下列说法正确的是( )
A.只有在t1 ℃时,NaCl和MgSO4的溶解度才相等
B.t1~t2 ℃,MgSO4的溶解度随温度升高而减小
C.在t2 ℃时,MgSO4饱和溶液的溶质质量分数最大
D.把MgSO4饱和溶液的温度从t3 ℃降至t2 ℃时,有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
下列晶体熔沸点由高到低的顺序正确的是( )
①SiC ②Si ③HCl ④HBr ⑤HI ⑥CO ⑦N2 ⑧H2
A.①②③④⑤⑥⑦⑧ B.①②⑤④③⑥⑦⑧
C.①②⑤④③⑦⑥⑧ D.⑥⑤④③②①⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子的外围电子排布式为 。
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 。
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③ 、④HCHO,其中碳原子采取sp2杂化的分子有
、④HCHO,其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为 形。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 。

(5)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如右上图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。
查看答案和解析>>
科目:高中化学 来源: 题型:
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。下图为RFC工作原理示意图,有关说法正确的是( )
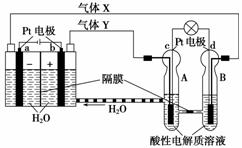
A.当有0.1 mol电子转移时,a极产生标准状况下1.12 L H2
B.左端装置中化学能转化为电能,右端装置中电能转化为化学能
C.c极上发生的电极反应是:O2+2H2O+4e-===4OH-
D.d极上发生还原反应,右端装置B中的H+可以通过隔膜进入A
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验能达到预期目的的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 向1 mL 0.2 mol·L-1 NaOH溶液中滴入2滴0.1 mol·L-1 MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1 FeCl3溶液,又生成红褐色沉淀 | 证明在相同条件下,溶解度Mg(OH)2>Fe(OH)3 |
| B | 向混有BaCO3沉淀的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| C | 两种一元碱溶液X和Y(X的pH比Y大1),分别加水稀释100倍后,pH相等 | 证明稀释前c(X)=10c(Y) |
| D | 测定等物质的量浓度的HF与HCl溶液的pH,后者较小 | 证明非金属性Cl>F |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 ( )
A. H2O(g)=H2(g)+ 1/2 O2(g) ΔH=+242 kJ/mol
1/2 O2(g) ΔH=+242 kJ/mol
B. 2 H2(g)+O2(g)=2 H2O(g) ΔH=-484 kJ/mol
C. H2(g)+1/2 O2(g)=H2O(g) ΔH=+242 kJ/mol
D. 2 H2(g)+O2(g)=2 H2O(g) ΔH=+484 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL 2 mol·L-1 FeCl3溶液和500 mL 2 mol·L-1明矾溶液分别滴入沸水中,加热制成分散系甲、乙,经测定,甲分散系中分散质的粒子直径大小在1~100 nm之间,乙分散系中分散质的粒子直径大小在10-9~10-7 m之间。下列关于甲、乙分散系的判断合理的是( )
A.在暗室里用一束明亮的“强光”照射甲、乙,发现甲有丁达尔效应,乙没有丁达尔效应
B.向甲、乙中分别滴加过量的氢氧化钠溶液,现象都是“先聚沉,后溶解”
C.向甲、乙中分别滴加过量的氢碘酸,最终现象分别是深褐色溶液、无色溶液
D.蒸干、灼烧FeCl3溶液和明矾溶液会得到对应的固体盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com