
【题目】短周期非金属元素B、C、N、O、P、S、Cl,可形成各种单质、化合物的分子。
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN![]() N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___。
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___。
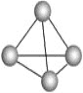
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为___和___(写1种,填化学式)。
(3)BF3和过量NaF作用可生成NaBF4,BF![]() 的空间立体构型为___。
的空间立体构型为___。
【答案】AD N2 CN-(或C![]() 、NO+) 正四面体
、NO+) 正四面体
【解析】
(1)A.N4由一种元素组成,是单质,故A错误;
B.N4分子是正四面体结构N—N键角为60°,故B正确;
C.N4分子中成键的原子相同,存在非极性键,故C正确;
D.N4=2N2,1molN4气体中含有6molN-N键,可生成2molN2,形成2molN≡N键,则1molN4气体转变为N2化学键断裂断裂吸收的热量为:6×167kJ=1002kJ,形成化学键放出的热量为1884kJ,所以反应放热,放出的热量为:1884kJ-1002kJ=882kJ,故应为放出882kJ热量,故D错误;
故答案为:AD;
(2)根据价电子迁移法和电子-电荷互换法得与CO互为等电子体的分子和离子分别为N2和CN-(或C![]() 、NO+),故答案为:N2;CN-(或C
、NO+),故答案为:N2;CN-(或C![]() 、NO+);
、NO+);
(3)BF![]() 的中心原子B为sp3杂化,空间立体构型为正四面体。故答案为:正四面体。
的中心原子B为sp3杂化,空间立体构型为正四面体。故答案为:正四面体。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH→CH3CH2CH2CHO
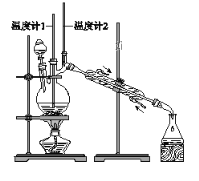
利用下图装置用正丁醇合成正丁醛。相关数据如下:
物质 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )
A. 为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B. 向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入1 molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应H2(g)+I2(g) ![]() 2HI(g),下列说法正确的是
2HI(g),下列说法正确的是
A. 保持容器容积不变,向其中加入1molH2,化学反应速率不变
B. 保持容器容积不变,向其中加入1molAr,化学反应速率增大
C. 保持容器内气体压强不变,向其中加入1molAr,化学反应速率不变
D. 保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),化学反应速率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.因为3O2![]() 2O3是吸热反应,所以臭氧比氧气的化学性质更活泼
2O3是吸热反应,所以臭氧比氧气的化学性质更活泼
B.太阳能、煤气、潮汐能是一次能源;电力、蒸汽、地热是二次能源
C.吸热反应就是反应物的总能量比生成物的总能量小的反应;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量少的反应
D.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=-566.0kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[实验化学]
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。

步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置中冷凝管的主要作用是________,锥形瓶中的溶液应为________。
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为_________。
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的______(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是_________。
(5)步骤4中采用减压蒸馏技术,是为了防止_____。
附表 相关物质的沸点(101kPa)
物质 | 沸点/℃ | 物质 | 沸点/℃ |
溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
苯甲醛 | 179 | 间溴苯甲醛 | 229 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,下列说法正确的是( )
CH3COO-+H+,下列说法正确的是( )
A.向体系中加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移
D.加水,平衡向正向移动,![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓硫酸和乙醇混合加热制取乙烯,下列说法正确的个数是( )

①浓硫酸只作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③反应温度缓慢上升至170℃
④用排水法或向下排气法收集乙烯
⑤圆底烧瓶中装的是4mL乙醇和12mL3mol/LH2SO4混合液
⑥温度计应插入反应溶液液面下,以便控制温度
⑦反应完毕后先熄灭酒精灯,再从水中取出导管
⑧该反应类型属于取代反应
⑨若a口出来的气体使溴水褪色,说明有乙烯生成
A.1B.2C.3D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨气可与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置(省略夹持装置及加热装置)可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是 ( )

A.试管A中加入的试剂为NH4Cl固体
B.反应中氧化剂和还原剂的物质的量之比为2 : 3
C.装置B中加入的物质可以是碱石灰或无水氯化钙
D.装置D中液体可以使干燥的红色石蕊试纸变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com