
| A. | ①③⑤ | B. | ①⑤⑦ | C. | ②⑥⑦ | D. | ①②④ |
分析 ①卤素单质性质很活泼,极易和其它物质反应;
②随着核电荷数增大,单质的熔沸点升高;
③随着核电荷数增大,单质的氧化性逐渐减弱;
④随核电荷数增加,非金属性减弱,对应气态氢化物稳定性逐渐减弱;
⑤最外层7个电子,所以易形成-1价离子;
⑥从上到下原子半径逐渐增大;
⑦从上到下非金属性逐渐减弱.
解答 解:①卤素原子最外层有7个电子,极易得电子生成8电子稳定结构,所以卤素单质性质很活泼,极易和其它物质反应,导致卤素只以化合态存在于自然界中,故正确;
②随着核电荷数增大,单质由气态→液态→固态,单质的熔沸点升高,故错误;
③随着核电荷数增大,卤素原子对最外层电子的吸引能力逐渐减小,导致单质的氧化性逐渐减弱,故错误;
④随核电荷数增加,非金属性减弱,对应气态氢化物稳定性逐渐减弱,故错误;
⑤最外层7个电子,所以易形成-1价的阴离子,故正确;
⑥从上到下原子半径逐渐增大,故错误;
⑦从上到下非金属性逐渐减弱,故正确;
故选B.
点评 本题考查了第VIIA族元素性质的相似性及递变性,根据元素周期律来分析解答即可,知道结构和性质的关系,题目难度不大.


科目:高中化学 来源: 题型:解答题

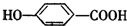 的化学方程式:
的化学方程式: .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 硫酸钠溶液和氯化钡溶液反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成的气体在标准状况下的体积为4.48 L | |
| B. | 硝酸只起到强氧化性作用 | |
| C. | 被还原的硝酸的物质的量为(0.2-a) mol | |
| D. | 反应后溶液中所含NO3-的物质的量为0.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应不属于氧化还原反应 | B. | CH3-CH=CH2发生氧化反应 | ||
| C. | 该反应属于加成反应 | D. | Xe是氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com