
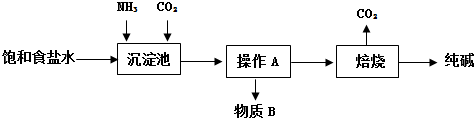
分析 侯氏制碱法的流程是在氨化饱和的氯化钠溶液里通CO2气体,因碳酸氢钠的溶解度比碳酸钠小,有碳酸氢钠沉淀生成,经过滤、洗涤干燥后,再将碳酸氢钠加热分解可得纯碱,同时生成的CO2气体循环利用,据此分析可解答;
(1)从溶液里得到不溶物的操作是过滤;
(2)氯离子的常见检验方法是在溶液里滴加硝酸银溶液,若有白色沉淀生成,再滴加稀硝酸看沉淀有无溶解判断;
(3)在同一温度下碳酸钠的溶解度比碳酸氢钠大,故侯氏制碱法直接得到的是碳酸氢钠.
解答 解:(1)利用过滤操作可从沉淀池中得到碳酸氢钠,故答案为:过滤;
(2)检验晶体中是否有氯离子,取少量晶体溶于水,加稀HNO3酸化,再滴加AgNO3溶液,若产生白色沉淀,该晶体中含有氯离子,故答案为:取少量晶体溶于水,加稀HNO3酸化,再滴加AgNO3溶液,若产生白色沉淀,该晶体中含有氯离子;
(3)因相同温度下,碳酸钠的溶解度大于碳酸氢钠,故向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,故答案为:相同温度下,碳酸钠溶解度比碳酸氢钠大.
点评 本题考查侯氏制碱法原理分析与应用,属基础性测试题,难度不大,建议学生多关注双基的复习.


科目:高中化学 来源: 题型:选择题
| 化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7, K2=5.6×l0-11 |
| A. | CH3COO-、CO32-、CN-在溶液中可以大量共存 | |
| B. | 向食醋中加入水可使CH3COOH的电离平衡向电离方向移动 | |
| C. | 相同物质的量浓度的Na2CO3和NaCN溶液,前者pH较大 | |
| D. | pH=a的上述3种酸溶液,加水后溶液的pH相同,则醋酸中加入的水最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | O.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min n/mol | 0min | 2min | 4min | 6min | 8min |
| n(X) | 0.2 | 0.15 | 0.1 | 0.1 | 0.05 |
| n(Y) | 0.6 | 0.45 | 0.3 | 0.3 | 0.5 |
| n(Z) | 0 | 0.1 | 0.2 | 0.2 | 0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 LCCl4中含Cl原子数目等于0.4NA | |
| B. | 2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| C. | 常温常压下,10 g 46%酒精水溶液中含氧原子总数为0.1NA | |
| D. | 1 mol甲基(-CH3)中含有电子的数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅熔点高硬度大,可用于制作半导体材料 | |
| B. | 氢氧化铝胶体具有吸附性,可用于制胃酸中和剂 | |
| C. | 人缺碘就会引起碘缺乏病,我国大部分地区都缺碘,因此80年代国家强制给食用盐中加入碘单质 | |
| D. | 硅胶具有吸水性,在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 mol | B. | 1/2 mol | C. | 1/3 mol | D. | 9 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com