
反应4NH3 + 5O2 == 4NO + 6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3
mol,则此反应的平均速度![]() (表示反应物的消耗速度或生成物的生成速度)为( )
(表示反应物的消耗速度或生成物的生成速度)为( )
(A)![]() (O
(O![]() )=0.01
)=0.01![]() (B)
(B)![]() (NO)=0.008
(NO)=0.008![]()
(C)![]() (H
(H![]() O)=0.003
O)=0.003![]() (D)
(D)![]() (NH
(NH![]() )=0.002
)=0.002![]()
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
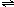 4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度
4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度. |
| Vx |
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com