BC
分析:A、二氧化硫具有还原性,溴单质具有氧化性,发生氧化还原反应生成硫酸和氢溴酸,溴化氢是强电解质;
B、酸式盐和碱反应,量少的全部反应;
C、依据醛基被氧化生成羧酸,银氨溶液被还原为单质银,依据电荷守恒和原子守恒分析判断;
D、惰性电极电解,阳离子在阴极上得到电子得到电子发生还原反应,阴离子在阳极上失去电子发生氧化反应;
解答:A、用二氧化硫水溶液吸收溴蒸气反应的离子方程式为:SO
2+Br
2+2H
2O=SO
42-+4H
++2Br
-;故A错误;
B、碳酸氢钠溶液中加入过量的氢氧化钡溶液,碳酸氢钠全部反应,反应的离子方程式为:Ba
2++OH
-+HCO
3-=BaCO
3↓+H
2O,故B正确;
C、用银氨溶液检验乙醛中的醛基:CH
3CHO+2Ag(NO
3)
2++2OH
-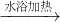
CH
3COO
-+NH
4++3NH
3+2Ag↓+H
2O,故C正确;
D、等物质的量浓度、等体积FeCl
3、NaBr、CuSO
4的混合溶液电解,最初发生的反应为,阳离子氧化性Fe
3+>Cu
2+>Na
+在阴极上得到电子得到电子发生还原反应,阴离子还原性顺序为Br
->Cl
->OH
->SO
42-在阳极上失去电子发生氧化反应;最初发生的反应为2Fe
3++2Br
-
2Fe
2++Br
2↑,故D错误;
故选BC.
点评:本题考查了离子方程式的书写方法和注意问题,主要是电荷守恒,错误判断,电解错误分析应用,氧化还原反应、强弱电解质的判断,题目难度中等.

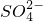 +2H++2HBr
+2H++2HBr CH3COO-+
CH3COO-+ +3NH3+2Ag↓+H2O
+3NH3+2Ag↓+H2O Cu↓+Cl2↑
Cu↓+Cl2↑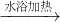 CH3COO-+NH4++3NH3+2Ag↓+H2O,故C正确;
CH3COO-+NH4++3NH3+2Ag↓+H2O,故C正确; 2Fe2++Br2↑,故D错误;
2Fe2++Br2↑,故D错误;
