
分析 原电池中,电子由负极流向正极,活泼金属作负极,负极上失去电子,正极上有气体或金属析出,负极的金属活泼性大于正极,以此来比较金属的活泼性.
解答 解:①A与B和CuSO4溶液组成原电池后,B极上附一层红色的铜,则B为正极,活泼性:A>B;
②B、C和CuSO4溶液组成原电池时,B的质量逐渐减轻,B为负极,A为正极,活泼性:B>C;
③A,D与CuSO4溶液组成原电池后,电子由D极经导线流向A极,则D失电子为负极,A为正极,活泼性:D>A;
④D、E与稀酸组成原电池后,在D极有大量气泡产生,则D为正极,E为负极,活泼性:E>D,
所以金属活泼性:E>D>A>B>C.
故答案为:E>D>A>B>C.
点评 本题考查原电池原理及金属活泼性的比较,明确活泼金属作负极,失去电子及电子的流向即可解答,题目较简单,侧重于基础知识的考查.


科目:高中化学 来源: 题型:选择题
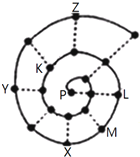 如图所示为“蜗牛”状的元素周期表,其中每个“•”代表一种元素,P点代表氢元素.下列说法正确的是( )
如图所示为“蜗牛”状的元素周期表,其中每个“•”代表一种元素,P点代表氢元素.下列说法正确的是( )| A. | Y元素对应的氢化物比Z元素对应的氢化物更稳定 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | M、K元素的离子半径大小顺序是M2+>K2- | |
| D. | 由K、L两种元素组成的化合物中不可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/K | 973 | 1173 | 1373 | 1573 |
| K | 1.47 | 2.15 | 3.36 | 8.92 |
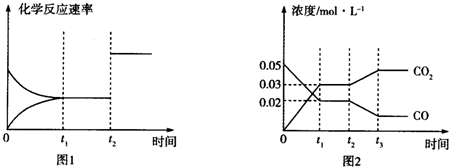
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分液时,先打开旋塞,待下层液体完全分出后,关闭旋塞,再从上口倒出上层液体 | |
| B. | 在油脂皂化反应实验中,用玻璃棒蘸取反应液滴入热水中,若无油滴浮于液面上,说明皂化反应已经完全 | |
| C. | 在中和热测定实验中,盐酸和NaOH溶液的总质量m g,反应前后体系温度变化△t℃,反应液的比热容为c J•g-1•℃-1,则生成1mol水放出的热量为cm△t×10-3kJ | |
| D. | 同一温度下,可通过观察出现浑浊的快慢来探究浓度对Na2S2O3与稀硫酸反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释,平衡左移,溶液颜色变浅 | |
| B. | 加入一定量的NaOH溶液,有红褐色沉淀产生,溶液颜色变浅 | |
| C. | 加入一定量的铁粉,充分振荡后,溶液颜色变浅 | |
| D. | 加入少量的KCl固体,平衡左移,溶液颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:m>n | B. | 氢化物的稳定性:n>p | ||
| C. | q的最高价氧化物的水化物为强酸 | D. | n在自然界中能以游离态存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com