

分析 硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH在2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl.
(1)硫酸的浓度为4.9g•L-1,结合n=$\frac{m}{M}$计算物质的量浓度,再根据pH=-lgc(H+)计算;
(2)c(NH4+)越大,NH4+水解程度越小;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,并洗涤、干燥;
(5)①H3AsO4是弱酸,电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀;
②Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O?HAsO42-+OH-,该步水解的平衡常数Kh=$\frac{c(HAs{{O}_{4}}^{2-})•c(O{H}^{-})}{c(As{{O}_{4}}^{3-})}$=$\frac{c(HAs{{O}_{4}}^{2-})•c(O{H}^{-})•c({H}^{+})}{c(As{{O}_{4}}^{3-})•c({H}^{+})}$=$\frac{Kw}{{K}_{3}}$=.
解答 解:硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH在2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl.
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=$\frac{\frac{4.9g}{98g/mol}}{1L}$=0.05mol/L,c(H+)=0.1mol/L,所以pH=-lg0.1=1,
故答案为:1;
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)大于NH4Cl溶液中的2倍,因c(NH4+)越大,NH4+水解程度越小,若(NH4)2SO4溶液中c(NH4+)等于H4Cl溶液中c(NH4+)的2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中$\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ 减小,
故答案为:减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2开始沉淀;
②Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O?HAsO42-+OH-,该步水解的平衡常数Kh=$\frac{c(HAs{{O}_{4}}^{2-})•c(O{H}^{-})}{c(As{{O}_{4}}^{3-})}$=$\frac{c(HAs{{O}_{4}}^{2-})•c(O{H}^{-})•c({H}^{+})}{c(As{{O}_{4}}^{3-})•c({H}^{+})}$=$\frac{Kw}{{K}_{3}}$=$\frac{1{0}^{-14}}{4.0×1{0}^{-12}}$=2.5×10-3,
故答案为:2.5×10-3.
点评 本题以化学工艺流程为载体,考查溶液pH计算、盐类水解影响因素、水解平衡常数计算、物质的分离提纯、对条件的控制与分析等,侧重于学生的分析、实验和计算能力的考查,液面考查的知识点较多,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
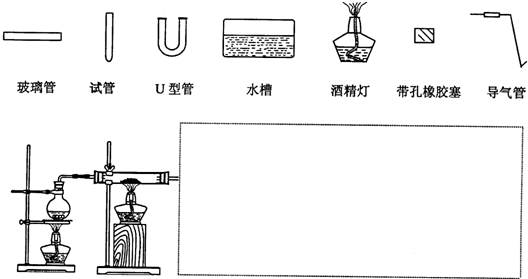
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
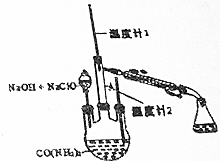 水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:
水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol Na2O2中所含的阴离子数为0.2NA | |
| B. | 常温常压下,5.6 g N2和CO混合物中所含有的原子总数为0.4 NA | |
| C. | 标准状况下,2.24 L H2O中含有的氧原子数目为0.1 NA | |
| D. | Cu和足量的浓硫酸反应产生4.48 L气体时,转移的电子数为0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素的金属性一定比ⅡA族元素的金属性强 | |
| B. | ⅥA族元素中氢化物最稳定的其沸点一定最高 | |
| C. | 非金属元素形成的化合物中也可能是离子化合物 | |
| D. | 离子化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 反应进行到5 s时,v(A)=v(B)=v(C)=v(D) | |
| B. | 反应进行到5 s时,B的平均反应速率为0.06mol/(L•s) | |
| C. | 反应进行到1 s时,v(A)=v(B) | |
| D. | 该反应的化学方程式为6A+2D?3B+4C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 榄香烯的分子式为C15H20 | |
| B. | 榄香烯属于芳香烃 | |
| C. | 1 mol 榄香烯最多能和6 mol H2反应 | |
| D. | 榄香烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com