
单官能团化合物EG是重要的有机化工原料,和有机物甲、乙、丙间存在如下的转化关系,丙为六元环状化合物,分子式为C4H4O4。
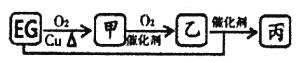
(无机反应物、生成物均已略去):
(1)写出EG→甲的化学反应方程式__________________________。
(2)甲乙丙中的一种可以发生银镜反应,写出它与足量银氨溶液反应的化学方程式_________________________________。
(3)化合物A的相对分子质量为84,其中含碳85.7%,含氢14.3%。A分子中所有的碳原子共平面,A的结构简式为______________________;
(4)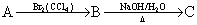 ,C和EG关系为_______________。
,C和EG关系为_______________。
 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
某同学设计如图所示的装置分别进行不同的探究实验(夹持装置已略去),请回答下列问题:

| 实验 | 药品 | 制取气体 | 量气管中液体 |
| Ⅰ | Cu、稀HNO3 | NO | H2O |
| Ⅱ | NaOH(s)、浓氨水 | NH3 | |
| Ⅲ | 电石、饱和NaCl溶液 | C2H2 | H2O |
| Ⅳ | 镁铝合金、NaOH溶液 | H2 | H2O |
(1)如何检验如图所示装置的气密性:________________________________________。
(2)该同学认为实验Ⅰ可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?__________(填“可行”或“不可行”),原因是_______________________。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是____________________________________,
打开开关K,产生的气体经验纯后点燃,现象是______________________________。
(4)实验Ⅱ中量气管中的液体最好是________(填字母编号,下同)。
a.浓NaOH溶液 b.氨水
c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需要吸收处理。以下各种尾气吸收装置中,适用于吸收NH3,而且能防止倒吸的有____________________________________________________________。


(5)本实验需对量气管进行多次读数,读数时应注意:①将实验装置恢复到室温,②__________________,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况下的体积,忽略滴入的液体体积对气体体积的影响):
| 编号 | 镁铝合金 质量 | 量气管 第一次读数 | 量气管 第二次读数 |
| ① | 1.0 g | 350.0 mL | 13.7 mL |
| ② | 1.0 g | 350.0 mL | 25.0 mL |
| ③ | 1.0 g | 350.0 mL | 14.3 mL |
根据表中数据,可计算出镁铝合金中铝的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是
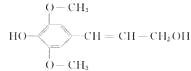
| A.芥子醇的分子式是C11H14O4属于芳香烃 |
| B.芥子醇分子中所有碳原子不可能在同一平面 |
| C.芥子醇不能与FeCl3溶液发生显色反应 |
| D.芥子醇能发生的反应类型有氧化、取代、加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A. 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ·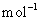 ,则
,则
 的
的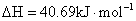
B. 已知MgCO3的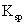 =6.82×
=6.82×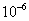 ,则所有含有固体MgCO3的溶液中,都有
,则所有含有固体MgCO3的溶液中,都有
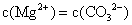 ,且
,且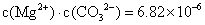
C. 已知:
| 共价键 | C—C | C=C | C—H | H—H |
| 键能/ | 348 | 610 | 413 | 436 |
则可以计算出反应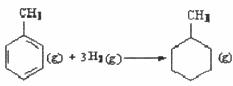 的
的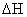 为
为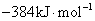
D. 常温下,在0.10 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离程度降低,溶液的pH减小
的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离程度降低,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
NM—3和D—58是正处于临床试验阶段的小分子抗癌药物,结构如下。关于NM—3和D—58的叙述,正确的是

A. NM—3和D—58互为同分异构体
B. NM—3和D—58都能与溴水反应,反应类型完全相同
C. 两者都能与NaOH溶液反应,且相同物质的量的NM—3和D—58消耗的NaOH的量相同
D. 都能和H2发生加成反应,且相同物质的量的NM—3和D—58最多消耗的H2物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.进行H2O和H2S的热分解实验,可确定S、O两种元素的非金属性强弱
B.根据非金属性强弱F>Cl,可以推测沸点HF>HCl
C.已知2C+SiO2 Si+2CO↑,说明C的非金属性比Si强
Si+2CO↑,说明C的非金属性比Si强
D.H2SO3的酸性比H2CO3的酸性强,说明S的非金属性比C强
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是一种重要的化工原料和新型燃料。
Ⅰ.工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g)  CH3OH(g) ΔH=-90.8 kJ·mol-1
CH3OH(g) ΔH=-90.8 kJ·mol-1
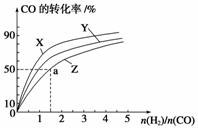
在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。下图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线Z对应的温度是________;该温度下上述反应的化学平衡常数为________;若增大H2的用量,上述反应的热效应最大值为_______________。
Ⅱ.下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
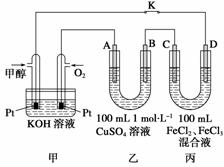
(1)甲中负极的电极反应式为________。
(2)乙中A极析出的气体在标准状况下的体积为________________。
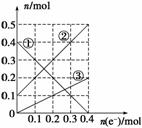
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如下图,则图中②线表示的是________的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要________ mL 5.0 mol·L-1 NaOH溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com