
| A£® | KCl | B£® | CuSO4 | C£® | AgNO3 | D£® | H2SO4 |
·ÖĪö ŅĄ¾Żµē½āŌĄķŗĶČÜŅŗÖŠĄė×ӷŵēĖ³Šņ·ÖĪöÅŠ¶Ļµē¼«·“Ó¦£¬ŅĄ¾Żµē½āÉś³ÉµÄ²śĪļ·ÖĪöČÜŅŗpH±ä»Æ£®
½ā“š ½ā£ŗA£®ÓĆ²¬µē¼«µē½āĀČ»Æ¼ŲČÜŅŗ£¬Éś³ÉĒāŃõ»Æ¼ŲŗĶĒāĘų”¢ĀČĘų£¬·“Ӧɜ³É¼ī£¬ČÜŅŗpHֵɿøߣ¬¹ŹAÕżČ·£»
B£®ÓĆ²¬µē¼«µē½āĮņĖįĶČÜŅŗ£¬Éś³ÉĶ”¢ŃõĘųŗĶĮņĖį£¬·“Ӧɜ³ÉĖį£¬ČÜŅŗpH½µµĶ£¬¹ŹB“ķĪó£»
C£®ÓĆ²¬µē¼«µē½āĻõĖįŅųČÜŅŗ£¬Éś³ÉŅų”¢ŃõĘųŗĶĻõĖį£¬·“Ӧɜ³ÉĖį£¬ČÜŅŗpH½µµĶ£¬¹ŹC“ķĪó£»
D£®ÓĆ²¬µē¼«µē½āĮņĖį£¬Ļąµ±ÓŚµē½āĖ®£¬ĮņĖįÅضČŌö“ó£¬ČÜŅŗpH½µµĶ£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²éĮĖµē½āŌĄķµÄ·ÖĪöÓ¦ÓĆ£¬Ć÷Č·µē½ā³Ų¹¤×÷ŌĄķ£¬×¼Č·ÅŠ¶ĻŃō¼«”¢Ņõ¼«·ÅµēĄė×ÓŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
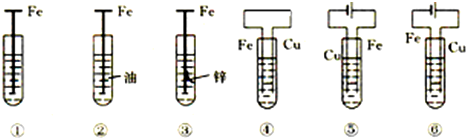
| A£® | ¢ŪŹĒĪžÉüŃō¼«µÄŅõ¼«±£»¤·Ø | |
| B£® | Čō½«¢ŽµÄCu¼«»»³É²»ČÜŠŌµē¼«£¬Ōņ¢ŽŹĒĶā¼ÓµēĮ÷µÄŅõ¼«±£»¤·Ø | |
| C£® | øÆŹ“æģµ½ĀżµÄĖ³ŠņĪŖ¢Ż£¾¢Ü£¾¢Ł£¾¢Ž£¾¢Ū£¾¢Ś | |
| D£® | ¢Ł·¢ÉśĪöĒāøÆŹ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.56 L¼×ĶéÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżĪŖ0.1NA | |
| B£® | ±ź×¼×“æöĻĀ£¬1mol SO3ŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ3NA | |
| C£® | 3mol NO2ŗĶ×ćĮæH2O·“Ó¦£¬×ŖŅĘ1 NAøöµē×Ó | |
| D£® | pH=1µÄĻ”ĮņĖįÖŠŗ¬ÓŠµÄH+ŹżĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=1µÄČÜŅŗÖŠ£ŗNa+”¢Fe2+”¢NO3-”¢SO42- | |
| B£® | ŗ¬Fe3+µÄČÜŅŗÖŠ£ŗK+”¢Mg2+”¢S2-”¢NO3- | |
| C£® | pH=13µÄČÜŅŗ£ŗNa+”¢K+”¢SiO32-”¢NO3- | |
| D£® | Ēæ¼īŠŌČÜŅŗÖŠ£ŗK+”¢Al3+”¢Cl-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖÄÖÖŌŖĖŲµÄŌ×Ó°ė¾¶£ŗA£¼B£¼D£¼C | |
| B£® | DŌŖĖŲ“¦ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµŚ3ÖÜĘŚµŚ¢öA×å | |
| C£® | B”¢DµÄ×īøß¼ŪŃõ»ÆĪļÖŠ£¬B”¢DÓėŃõŌ×ÓÖ®¼ä¾łĪŖĖ«¼ü | |
| D£® | Ņ»¶ØĢõ¼žĻĀ£¬Dµ„ÖŹÄÜÖĆ»»³öBµ„ÖŹ£¬Cµ„ÖŹÄÜÖĆ»»³öAµ„ÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 56gĢś±»Ńõ»ÆŹ±£¬Ź§Č„µē×ÓŹżÄæŅ»¶ØŹĒ2NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬71g Cl2ÖŠŗ¬µē×Ó×ÜŹżĪŖ34NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24L SO3ÖŠ£¬ŗ¬·Ö×Ó×ÜŹżĪŖ0.1NA | |
| D£® | CnH2n+2·Ö×ÓÖŠŗ¬ÓŠ¹²¼Ū¼üŹżĪŖ£Ø3n+1£©NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖį | B£® | Ēā·śĖį | C£® | ÉÕ¼ī | D£® | ±„ŗĶŹ³ŃĪĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
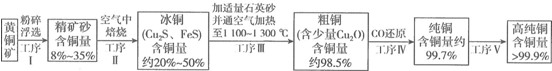
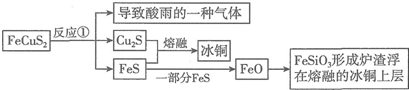
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £»
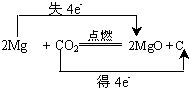
£»
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com